液流蓄电系统通常又被称为氧化还原液流储能系统(Redox-Flow Cell或Redox-flow Cell for Energy Storage Systems,液流蓄电站或液流电池),是由ThallerL.H(NASA Lewis Research Center,Cleveland,United States)于1974年提出的一种电化学储能原理。
如图3-15所示,液流蓄电系统由电堆、电解质溶液,以及电解质溶液储供体系、系统控制体系、充放电体系等部分组成。液流蓄电系统的核心是电堆,由数十节乃至数百节进行氧化、还原反应。实现充、放电过程的单电池按特定要求串、并联而成,结构与燃料电池的电堆有类似之处。与通常蓄电池中活性物质被包含在电池的正负极内不同,液流电池中的正、负极氧化还原活性物质,分别溶解于装在两个储液罐中的电解质溶液中,各用一个泵使溶液流经液流电池。电解质在电堆中循环流动,并在离子交换膜两侧的多孔电极上分别发生还原和氧化反应。反应过程中,为了在电池内部形成闭合回路,以及保持膜两侧溶液的电荷平衡,必定有一种离子同步地由膜的一侧通过离子交换膜向另一侧溶液迁移。不同活性物质组合成的电化学体系,各有其特定的反应历程、反应产物和迁移离子。
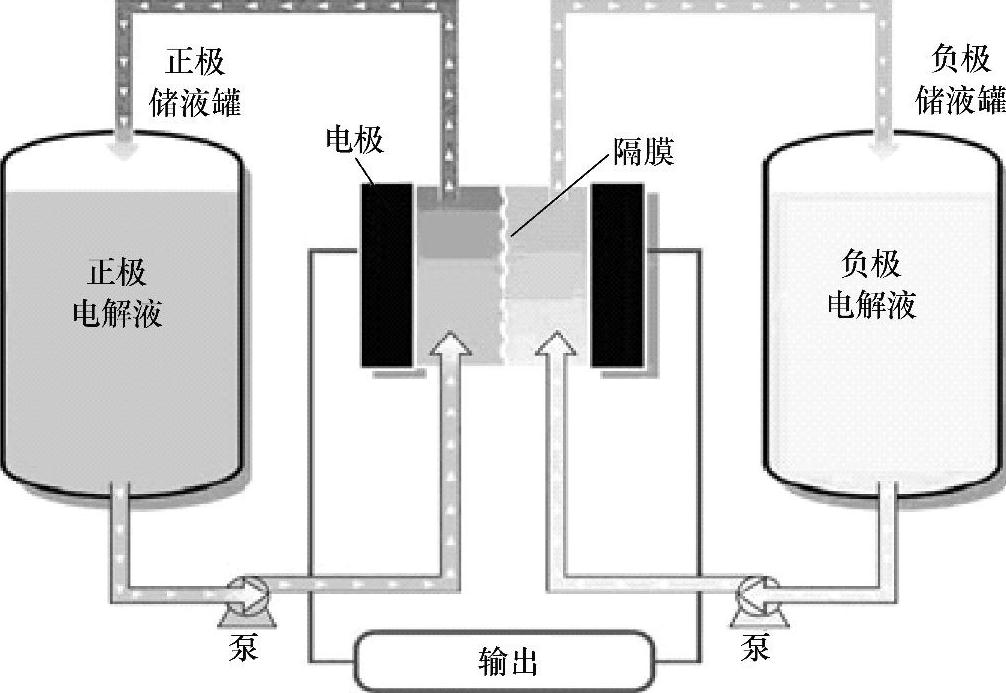
图3-15 钒电池基本工作原理示意图
钒电池以溶解于一定浓度硫酸溶液中的不同价态的钒离子为正负极电极反应活性物质。电池正负极之间以离子交换膜分隔成彼此相互独立的两室。通常情况下钒电池正极活性电对为VO2+/VO+,负极为V2+/V3+。电极上所发生的反应如下:(https://www.xing528.com)
正极:VO2++H2O-e→VO+2+2H+
负极:V3++e→V2+
电池总反应:VO2++H2O+V3+→VO+2+V2++2H+
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




