1)催化NaBH4还原4-NP的反应
为了测试合成粒子的催化性能,过量NaBH4还原4-NP作为测试反应。该反应溶液颜色及紫外吸收变化如图8.4.14所示,4-NP溶液呈淡黄色并在317 nm出表现出明显的紫外特征吸收峰。加入NaBH4后,溶液的颜色变为亮黄色,同时吸收峰明显红移至400 nm处,这是由于在碱性条件下,对硝基苯酚中的酚羟基发生电离形成对硝基苯酚离子![]() 。催化后亮黄的溶液变为无色,生成物4-AP的紫外特征吸收峰在300 nm处。
。催化后亮黄的溶液变为无色,生成物4-AP的紫外特征吸收峰在300 nm处。
室温条件下,不同纳米粒子催化NaBH4还原4-NP的紫外吸收曲线如图8.4.15所示。由催化曲线可知,即使反应60 min对照组(仅有NaBH4和4-NP)的紫外吸收峰在400 nm处仍没有明显的变化,且在300 nm处也没有出现4-AP的特征吸收峰,说明NaBH4还原4-NP的反应在没有催化剂存在的条件下很难进行。当加入催化剂后,对氨基苯酚离子在400 nm处吸收峰的强度迅速降低,同时在300 nm处产生4-AP的特征吸收峰。对比可知,使用的催化剂中含有金时,NaBH4还原4-NP的紫外吸收曲线会在300 nm处立即产生4-AP的特征吸收峰,而对于测试中的其他催化剂,虽然400 nm处吸收峰的强度迅速降低,但300 nm处并没有立即产生特征吸收峰,说明金属Ni对NaBH4还原4-NP反应的催化存在诱导期,曾有文献报道在Ni-Au复合结构中4-NP分子更加倾向于与金进行相互作用。
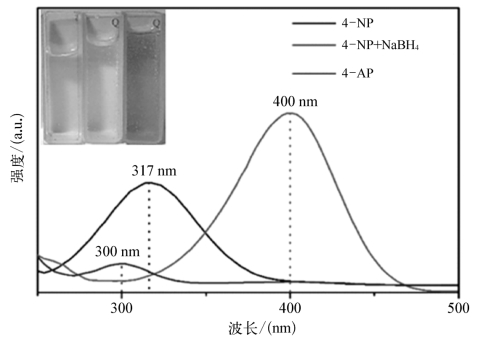
图8.4.14 室温条件下(26±1℃),4-AP及4-NP(0.1 mM)加入NaBH4(0.2 M)前后的紫外吸收谱图。插图为溶液颜色变化的相应照片
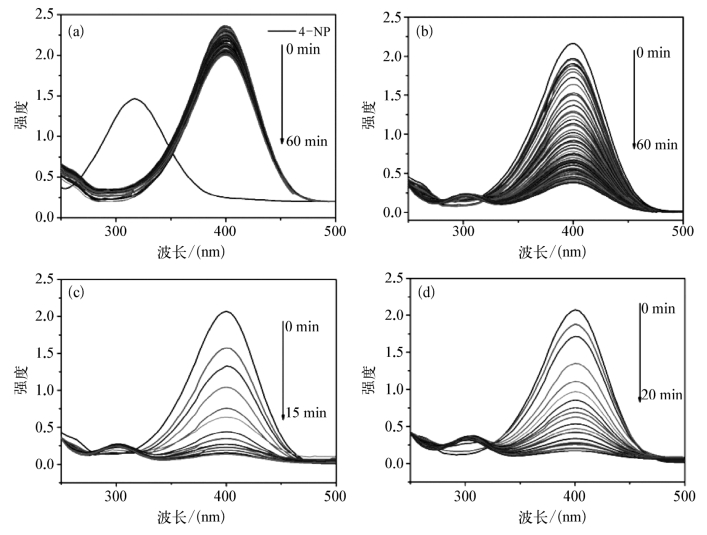
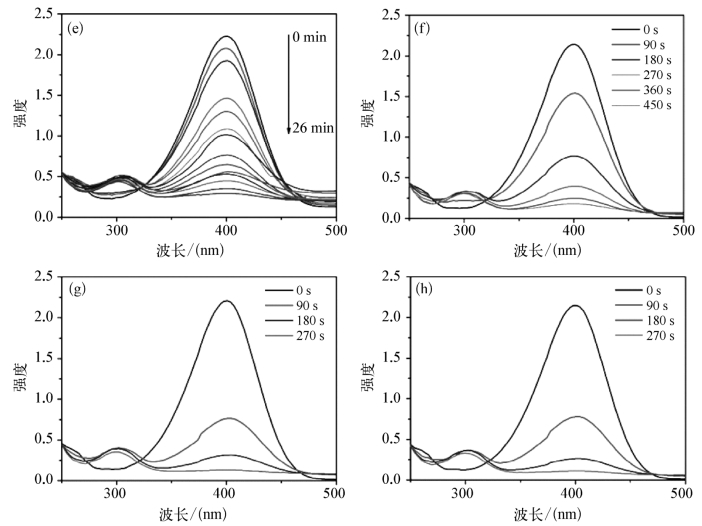
图8.4.15 室温条件下,不同纳米粒子(0.3 mL,1 mg/mL)催化NaBH4(0.2 M)还原4-NP(3 mL,0.1 mM)的紫外吸收谱图
(a)对照组;(b)还原氧化石墨烯;(c)镍-金;(d)还原氧化石墨烯-金;(e)还原氧化石墨烯-镍;(f)还原氧化石墨烯-镍-金-1h;(g)还原氧化石墨烯-镍-金3h;(h)还原氧化石墨烯-镍-金-6 h
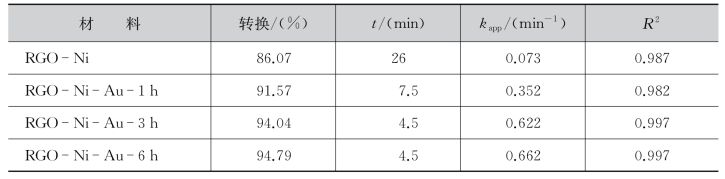
不同纳米粒子催化NaBH4还原4-NP反应的转化率、催化时间(t)、表观速率常数(kapp)及相关系数(R2)列于表8.4.1。其中,RGO-Ni-Au-6 h(3 h)、RGO-Ni-Au-1 h、Ni-Au、RGO-Au及RGO-Ni完成催化的时间分别为4.5 min、7.5 min、15 min、20 min和26 min。分析图8.4.16(a)可知,与对照组相比我们发现RGO本身对NaBH4还原4-NP反应也有催化作用,且在60 min内的催化转换率为82.54%。对比各组测试的转化率得出结论,RGO负载的双金属纳米粒子在催化5 min内的转换率(>80%)均高于RGO负载的单金属RGO-Ni(34.29%)和RGO-Au(53.25%)或无载体的Ni-Au纳米粒子(69.34%),这是由于载体RGO良好的导电性促进了催化反应中的电子传输过程,利用自身石墨烯片层结构中的共轭π键将电子快速传输给4-NP。尽管无载体Ni-Au纳米粒子催化时间(15 min)长于RGO-Ni-Au体系,但是优于RGO负载的单金属RGO-Ni和RGO-Au体系。这一点充分说明了RGO作为载体不仅防止了金属纳米粒子的团聚,同时对金属纳米粒子的协同作用也有重要的影响。此外,纳米粒子对反应的催化活性随着复合纳米粒子中金含量的增加为增强。由图8.4.9 EDX能谱分析可知,RGO-Ni-Au-6 h(1.97)的金含量率高于RGO-Ni-Au-3 h(1.68),但两者完成催化的时间相同均为4.5 min,这可能是由于结构不同造成的。对比RGO-Ni-Au-6 h(见图8.4.4(d))和RGO-Ni-Au-3 h(见图8.4.4(c))的SEM可知,RGO-Ni-Au-6 h样品中金属Ni和Au多以核壳结构(Ni@Au)存在于载体RGO表面,因此在反应过程中更多的是金外壳参与催化,而RGO-Ni-Au-3 h样品中金属镍和金的复合形式能够使两种金属同时参与催化过程,从而表现出良好的协同作用。这一结果表明催化性能与催化剂的组成、结构及粒子大小等因素密切相关。
众所周知,当NaBH4用量过量时,NaBH4还原4-NP的反应符合准一阶反应动力学方程。为了进一步对比研究制备纳米粒子的催化性能,通过计算-ln(C/C0)与反应时间t之间的线性关系得出纳米粒子催化反应的表观速率常数kapp,其中C和C0分别为催化时间t及初始时4-NP的浓度。如图8.4.16(b)和表8.4.1所示-ln(C/C0)与反应时间t之间呈现良好的线性关系,且相关系数R2均大于0.96,这对实际催化应用具有十分重要的指导意义。不同催化纳米粒的kapp值比较为RGONi-Au-6 h(0.662 min-1)≈RGO-Ni-Au-3 h(0.622 min-1)>RGO-Ni-Au-1 h(0.352 min-1)>Ni-Au(0.169 min-1)>RGO-Au(0.126 min-1)>RGO-Ni(0.073 min-1)。虽然RGONi-Au-6 h与RGONi-Au-3 h完成催化的时间相同,但由kapp值可以看出RGONi-Au-6 h的催化性能率优于RGONi-Au-3 h。对比kapp值分析,RGO-Ni-Au-3/6 h复合纳米粒子的kapp值分别是Ni-Au,RGO-Au和RGO-Ni的4、5和9倍,这一结果表明通过与RGO复合,可明显提高金属镍和金的催化性能。
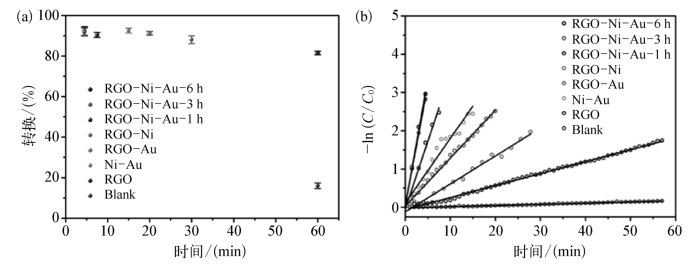
图8.4.16 室温条件下,不同纳米粒子(0.3 mL,1 mg/mL)催化NaBH4(0.2 M)还原4-NP(3 mL,0.1 mM)的(a)转化率和(b)-ln(C/C0)对时间的拟合曲线
表8.4.1 NaBH4还原4-NP反应的转化率、催化时间(t)、表观速率常数(kapp)及相关系数(R2)
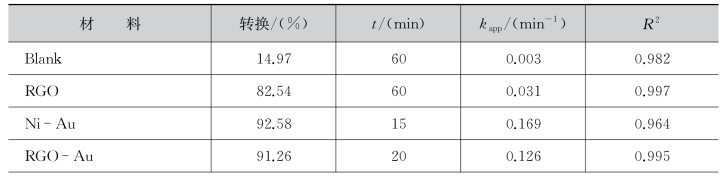
(续表)
2)反应温度对催化性能的影响
为了探究不同反应温度条件下催化剂的活性,在其他催化条件不变的情况下对RGO-Ni-Au-3 h在288 K和308 K条件下催化NaBH4氢化还原4-NP的反应进行测试。测试结果如图8.4.17和表8.4.2所示。对比不同温度下纳米催化剂的反应速率常数可知,所制备纳米粒子的催化性能随温度升高而增加,但是各催化剂的催化性能高低顺序并未改变。
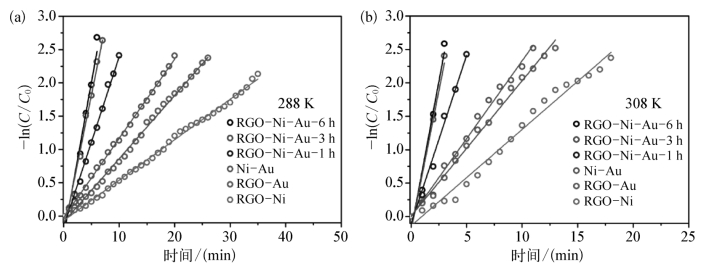
图8.4.17 不同温度条件下,不同纳米粒子(0.3 mL,1 mg/mL)催化NaBH4(0.2 M)还原4-NP(3 mL,0.1 mM)的-ln(C/C0)对时间的拟合曲线(a)288 K和(b)308 K
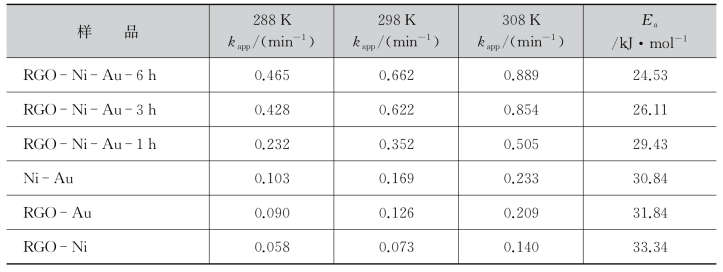
表8.4.2 不同温度条件下,不同纳米粒子催化NaBH4还原4-NP反应的速率常数
在不同温度下,所制备的纳米催化剂对于催化NaBH4还原4-NP反应的-ln(C/C0)对时间的拟合曲线均呈现良好的线性关系(如图8.4.16(b)和图8.4.18所示)。因此根据阿伦尼乌斯(Arrhennius)式(8-1)计算反应的活化能:
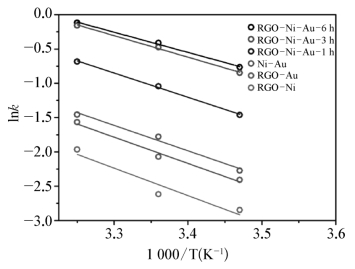
图8.4.18 不同温度条件下所制备的纳米催化剂催化NaBH4还原4-NP反应的ln k对1 000/T拟合曲线
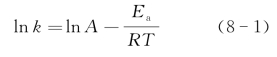
其中,k即为前述的表观反应速率常数kapp,A为指前因子。以ln k对1 000/T进行拟合作图,由直线的斜率可得表观活化能Ea,由截距可得指前因子A。所制备纳米催化剂RGONi-Au-1 h、RGO-Ni-Au-3 h、RGO-Ni-Au-6 h、Ni-Au、RGO-Au和RGO-Ni对应的反应活化能Ea分别为24.53 kJ·mol-1、26.11 kJ·mol-1、29.43 kJ·mol-1、30.84 kJ·mol-1、31.84 kJ·mol-1和33.34 kJ·mol-1。其中RGO-Ni-Au-6 h催化时反应的活化能最低,与其具有最高催化活性相对应。
3)催化剂用量对催化性能的影响(https://www.xing528.com)
在其他测试条件不变的情况下,我们通过改变催化剂的用量来探究催化剂的浓度对NaBH4还原4-NP反应的影响,其中所选用催化剂RGO-Ni-Au-3 h的用量分别为0.1 mL、0.2 mL、0.3 mL、0.35 mL和0.4 mL。结果如图8.4.19所示,当催化剂的用量为0.1~0.3 mL时,反应的kapp(min-1)值明显增加,当用量为0.3 mL时增至0.622 min-1。当催化剂的用量超过0.3 mL(0.35 mL和0.4 mL),反应的kapp(min-1)值仅有略微的增加,用量为0.4 mL时的kapp值为0.637 min-1,与用量0.3 mL时相比仅提高了0.015,这说明催化剂的用量对于该实验条件下NaBH4还原4-NP的反应已经饱和,即使再进一步增加催化剂的用量,反应的kapp值也没有更多的提高。因此,我们认为在本章实验条件下,采用0.3 mL催化剂(1 mg/m L)这一优化值能够充分催化NaBH4还原4-NP的反应。
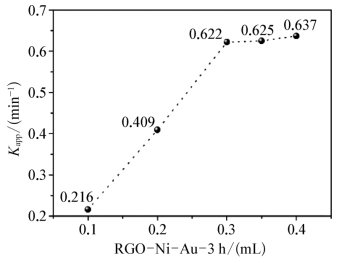
图8.4.19 室温条件下,不同用量的RGONi-Au-3 h(1 mg/mL)催化NaBH4(0.2 M)还原0.125 mM 4-NP反应的kapp(min-1)值
催化NaBH4还原4-NP反应的机理如图8.4.20所示。该反应的进行主要取决于电子由供体![]() 传递给受体4-NP,这一过程明显受NaBH4水解速率的影响,如式(8-2):
传递给受体4-NP,这一过程明显受NaBH4水解速率的影响,如式(8-2):
![]()
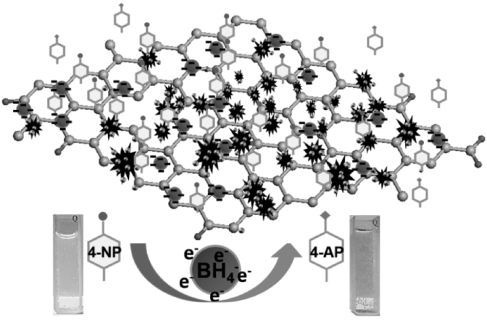
图8.4.20 反应机理示意
曾有文献报道基于过渡金属的复合纳米粒子能够催化NaBH4的水解。此外,在水溶液的催化体系中,![]() 离子首先吸附在催化剂的表面,催化剂一方面促进NaBH4的水解,另一方面将
离子首先吸附在催化剂的表面,催化剂一方面促进NaBH4的水解,另一方面将![]() 的电子传递给
的电子传递给![]() 离子同时发生氢化还原反应。因此,在催化NaBH4还原4-NP的反应过程中,RGO-Ni-Au复合纳米粒子主要是作为电子传递的桥梁。
离子同时发生氢化还原反应。因此,在催化NaBH4还原4-NP的反应过程中,RGO-Ni-Au复合纳米粒子主要是作为电子传递的桥梁。
基于以上的原理讨论,我们分析了催化活性增强的原因:从RGO载体分析①RGO载体独特共轭π键电子结构使得催化剂RGO-Ni-Au具有较高的电子迁移率,因此可以加速催化过程中的电子传输,这一点对于提升NaBH4还原4-NP的反应速率有十分重要的影响;②与无载体的Ni-Au催化粒子相比,载体RGO不仅能够防止Ni-Au纳米粒子的团聚而提高其催化稳定性,同时提供了比表面积较大的反应平台(见图8.4.13,BET 28.5 m2 g-1);③4-NP分子与载体RGO片层间的π-π堆积作用增加了载体表面Ni-Au纳米粒子周围4-NP分子的浓度,这能够促进4-NP分子与金属粒子之间的充分接触。然而,我们在不加入NaBH4的条件下,测试RGO对4-NP分子的吸附情况发现RGO对于4-NP并没有表现出明显的吸附行为(如图8.4.21所示)。因此,我们认为这一性能对于促进该电子诱导的氢化还原反应贡献较少。从Ni-Au复合纳米粒子角度分析①该复合纳米粒子除了可以像载体RGO一样起到电子传输的作用,文献中还曾指出金属纳米粒子在氢化物电子传输的过程中具有储存电子的能力;②基于无载体Ni-Au纳米粒子的催化活性优于RGO负载的单金属纳米粒子(RGO-Ni和RGO-Au),我们可以得出结论,RGO-Ni-Au催化体系中金属镍和金之间强烈的协同作用对复合纳米粒子的催化活性起到了至关重要的作用。
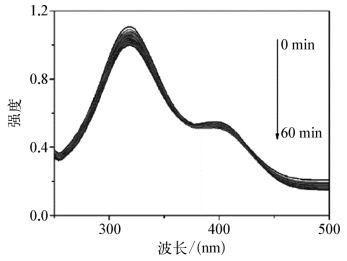
图8.4.21 室温在无NaBH4的条件下,RGO(0.3 mL,1 mg/mL)吸附4-NP(3 mL,0.1 mM)的紫外吸收曲线
为了与报道中结构相近的催化纳米粒子进行比较,反应速率常数按照催化剂的用量进行归一化,计算公式定义如下所示:
![]()
其中kapp为反应的表观速率常数(单位,min-1),m为催化剂的用量(单位,mg)。如表8.4.3所示,我们制备的催化剂催化NaBH4还原4-NP反应的活性优于部分相关报道的最佳结果,但与个别RGO负载型的纳米催化剂和贵金属合金相比,我们制备的RGO-Ni-Au复合纳米粒子的催化性能仍有待提高。但需要强调的是,我们的合成方法省时经济耗能少且催化效率高,更加适合工业化大规模还原4-NP。
表8.4.3 同类型催化剂催化NaBH4还原4-NP反应的速率常数及催化活性参数比较
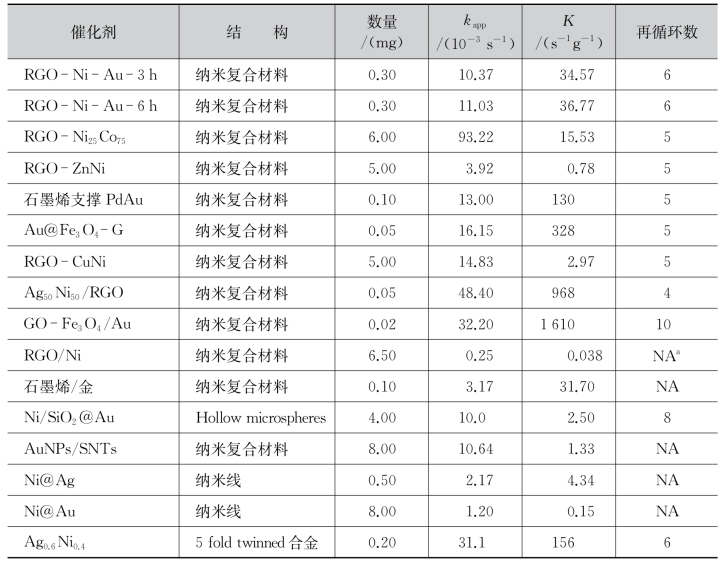
NAa,无法使用。
4)RGO-Ni-Au-3 h催化稳定性探究
为了进一步评估制备的复合纳米粒子的催化性能,我们对RGO-Ni-Au-3 h催化NaBH4还原4-NP反应的重复使用稳定性进行测试。每次催化结束后,用一个外加磁场回收复合纳米粒子,回收的固体利用无水乙醇进行超声清洗后放置在真空干燥箱中干燥(30℃),得到的干燥固体用以下一个催化测试。结果如图8.4.22所示,经过6次循环使用后,RGO-Ni-Au-3 h复合纳米粒子对NaBH4还原4-NP的反应仍具有良好的催化活性,催化转换率仍可达90%。但是需要指出的是,完成催化的时间由第一次的4.5 min增至第6次的18 min,这主要是由每次回收过程中不可避免的催化剂损失造成的。因此,在今后的工作中我们应该进一步改善纳米粒子催化剂的使用形式,在不影响催化性能的条件下可将粉末状态的催化剂制备成膜片、线状或者是空心的块体结构,这样的设计在理论上可降低多次回收使用过程中催化剂的损失。
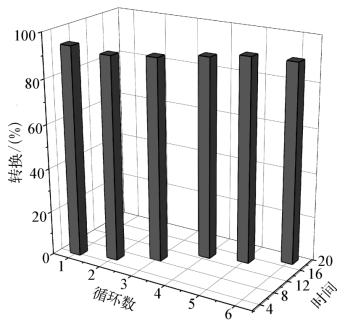
图8.4.22 室温条件下,RGO-Ni-Au-3 h催化NaBH4还原4-NP反应的重复使用稳定性测试
5)催化NaBH4降解有机染料
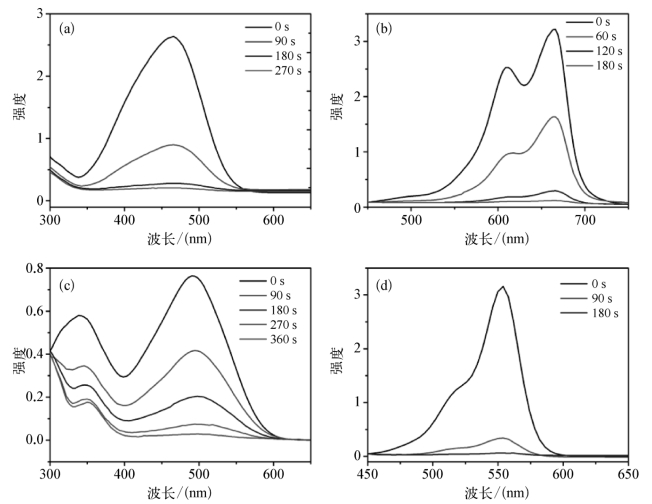
图8.4.23 室温条件下RGO-Ni-Au-3 h(0.3 mL,1 mg/mL)催化NaBH4(0.4 mL,0.2 M)降解不同染料的紫外吸收曲线
(a)MO;(b)MB;(c)CR;(d)RhB。其中MB的浓度为0.062 5 mM,RhB、CR和MO的浓度分别为0.125 mM
为了进一步探究RGO-Ni-Au对NaBH4诱导的反应的催化作用,我们对RGO-Ni-Au-3 h催化NaBH4降解染料的反应进行测试。选用MO、MB、CR和RhB四种结构差别较大的代表性染料进行降解。其中MB的浓度为0.062 5 mM,RhB、CR和MO的浓度分别为0.125 mM。催化结果如图8.4.23所示,加入RGO-Ni-Au-3 h后,NaBH4降解染料的反应立即开始进行并没有观察到存在明显的诱导期,而且在催化剂加入后的1.5 min内染料的特征吸收峰强度下降最为明显。RGO-Ni-Au-3 h复合纳米粒子催化NaBH4降解MO、MB、CR和RhB染料的时间分别为4.5 min、3 min、6 min和3 min,并且降解率高达99%(见图8.4.24),这表面在RGO-Ni-Au-3 h作为催化剂的条件下,NaBH4完全降解了这四种染料。综合催化效率和降解率分析,在该催化条件下(温度,各物质浓度),实际应用中可将催化降解的时间控制在3 min,即可达到效果。需要指出的是RGO-Ni-Au-3 h对于不同染料的催化降解效率不同是由于染料分子自身的结构、大小及电性差别造成的。因此,我们认为制备的RGO-Ni-Au复合纳米粒子对于NaBH4诱导的反应(还原和氧化)具有良好的催化性能。
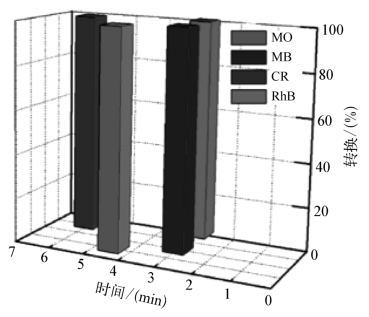
图8.4.24 室温条件下RGO-Ni-Au-3 h(0.3 mL,1 mg/mL)催化NaBH4(0.4 mL,0.2 M)降解不同染料的降解率
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




