多元酸在溶液中发生逐级解离,是一种复杂的酸碱平衡系统,即便是一种二元酸,在严格处理时,得到的也是一个[H+]的四次方程,这在化学上很少有意义。下面主要讨论如何进行简化处理。
现以二元酸H2A为例。在水溶液中可选H2A和H2O为参考水准,质子平衡方程式为
因溶液呈酸性,故可略去[OH-]项,得到简化质子平衡式,代入有关平衡常数得
若2K a2/[H+]≪1,可将其略去,则
该式与计算一元弱酸溶液[H+]的公式(4.37)类似,实际上是忽略多元酸的第二级解离,将其近似地按一元弱酸处理。
例4.11 计算0.10 mol·L-1丁二酸(C4H6O4,又称琥珀酸)溶液的pH。
解:已知K a1=K a(C4H6O4)=6.2×10-5,![]() =2.3×10-6,c a=c(C4H6O4)=0.10 mol·L-1,则c a/K a1=1 613>500,可按一元酸的最简式计算:
=2.3×10-6,c a=c(C4H6O4)=0.10 mol·L-1,则c a/K a1=1 613>500,可按一元酸的最简式计算:
这时,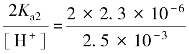 =1.8×10-3≪1。说明符合将多元酸作为一元酸近似处理条件。(https://www.xing528.com)
=1.8×10-3≪1。说明符合将多元酸作为一元酸近似处理条件。(https://www.xing528.com)
例4.12 计算0.10 mol·L-1酒石酸溶液的pH。
解:已知K a1=9.2×10-4,K a2=4.3×10-5,c a=c(C6 H6 O6)=0.10 mol·L-1,c a/K a1=108<500,应按一元酸的近似式(4.36)计算:
这时,
可见,即便像丁二酸和酒石酸这些K a1和K a2相差不大的多元酸(Δp K a仅为1.4和1.3),只要溶液的浓度不是太稀,均可按一元酸近似处理。类似地,多元碱溶液亦可按一元弱碱溶液计算其[OH-],只是以K b1代替式(4.39)和式(4.40)中的K b。
例4.13 计算0.10 mol·L-1 Na2CO3溶液的pH。
解:Na2CO3溶液是多元弱碱![]() 溶液,则
溶液,则
按题意,c b=![]() =0.10 mol·L-1,因c b/K b1>500,故可按最简式计算:
=0.10 mol·L-1,因c b/K b1>500,故可按最简式计算:
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




