1.什么是偶合反应?偶合反应属于哪种反应类型?为什么偶合反应总是发生在重氮盐与酚类或芳胺之间?
●答 重氮盐在中性、弱酸或弱碱性介质中与芳胺或酚类作用,由偶氮基将两个分子偶联起来,生成偶氮化合物的反应称为偶合反应。
偶合反应属于亲电取代反应。由于重氮阳离子是弱的亲电试剂,故只有苯环上电子云密度高的芳胺或酚类,才能与之顺利进行反应。
2.反应介质对反应是否有影响?重氮盐与酚类和芳胺偶合时,应在什么介质中更加有利?为什么?
●答 反应介质对偶合反应是有影响的。重氮盐与酚类的偶合反应,在弱碱性介质中进行有利。因为在碱性介质中,酚转变成苯氧负离子,苯氧负离子的苯环上电子云密度比酚中苯环上的电子云密度要高,更容易受重氮阳离子的进攻。但溶液的碱性不宜太强,否则重氮阳离子将转变为重氮酸或重氮盐而不进行偶合反应。

重氮盐与芳胺进行的偶合反应,在中性或弱酸性介质中进行更有利。因为在强酸性介质中,芳胺将转变为铵盐,导致芳环的电子云密度太低,而不能进行偶合反应。
3.在制备重氮盐(如制备氯化重氮苯)时,为什么要在强酸介质中进行?并且强酸要适当过量?
●答 制备重氮盐时,要用过量的酸,是因为重氮盐在酸性介质中更加稳定。另外,过量的酸可与未重氮化的少量芳胺形成铵盐(ArNH3+),从而防止重氮盐与未反应的芳伯胺发生偶合反应。
重氮化反应之所以要在强酸性介质中进行,是因为芳伯胺的碱性太弱,只有与强酸才能形成稳定的盐。为防止生成的重氮盐与未反应的芳伯胺偶联,同时,为了防止生成的重氮盐离子进攻未反应的芳伯胺的氮离子形成重氮氨基苯。例如,
![]()
因此,重氮化反应必须在强酸中进行。
4.重氮化反应为什么在低温下进行?
●答 若反应温度较高,一方面亚硝酸分解的速度加剧,使重氮化反应不完全;另一方面,温度过高会导致生成的重氮盐易水解成苯酚:

所以,重氮化反应通常在低温中进行(一般是0~5℃)。
5.在进行重氮反应时,为什么加NaNO2溶液(直接法重氮化)或加盐酸溶液(倒转法重氮化)时反应要慢?
●答 在芳伯胺与盐酸的混合液中加入Na2NO2溶液称为直接法重氮化。在芳伯胺与碱的混合液中加计算量的Na2NO2溶液,最后再滴加盐酸,直至重氮化作用完全的操作称为倒转法重氮化。在进行重氮化反应时,最后无论是加Na2NO2溶液还是加盐酸溶液都要慢。因为重氮化反应作用较慢,同时,重氮化反应是个放热反应。加料快时,一方面亚硝酸积聚,易于分解;另一方面,会使溶液温度升高,对重氮化反应不利。
6.在制备甲基橙时,难溶于酸的对氨基苯磺酸大多采用倒转法重氮化,在缓慢加入盐酸溶液的同时,为什么要不断搅拌?
●答 在对氨基苯磺酸钠和NaNO2混合液中,缓慢加入盐酸溶液,一方面使NaNO2生成亚硝酸(NaNO2+HCl—→HNO2+NaCl);另一方面,使对氨基苯磺酸钠分解为对氨基苯磺酸而产生细粒状沉淀析出,并立即与亚硝酸发生重氮化反应,生成对氨基苯磺酸的重氮盐。为了使对氨基苯磺酸完全重氮化,在反应过程中必须不断搅拌。
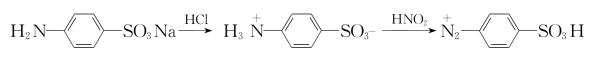
7.在制备重氮盐时,为什么要把对氨基苯磺酸变成钠盐后,再加NaNO2和浓盐酸?如果改为先将对氨基苯磺酸与浓盐酸混合,再加NaNO2溶液进行重化反应,这样做行不行?为什么?
●答 对氨基苯磺酸是一种两性有机物,其酸性比碱性强,以酸性内盐存在,它能与碱形成盐,而不与酸作用。重氮化反应又必须在酸性溶液中完成。因此,在进行重氮化反应时,要先将对氨基苯磺酸与碱作用,变成水溶性较大的对氨基苯磺酸钠,然后再加NaNO2和盐酸。
若改成先与盐酸混合,再滴加NaNO2溶液是不行的。因为对氨基苯磺酸不溶于酸,此时,对氨基苯磺酸以固体形式沉在下层、盐酸在上层。当加入NaNO2溶液时,上层溶液(盐酸)与之生成亚硝酸。亚硝酸易分解,而下层的固体最多只能在两相界面处接触到亚硝酸发生重氮化。因此,重氮化效果差,甚至不能进行重氮化。(https://www.xing528.com)
8.在制备甲基橙时,在重氮化过程中亚硝酸过量是否可以?如何检验其是否过量?又如何销毁过量的亚硝酸?
●答 亚硝酸过量不好。因为亚硝酸能起氧化和亚硝化作用,同时还会引起一系列副反应。
当重氮化反应完成后,溶液中若有过量的亚硝酸存在,可用淀粉-KI试纸
检验:
2HNO2+2KI+2HC—→I2+2H2O+2KCl
析出的碘使淀粉变蓝。
注意以下问题:
(1)反应液应呈酸性。
(2)淀粉-KI试纸是否灵敏(用NaNO2溶液酸化后试验)。(3)只有在反应液接触试纸后15~20s内呈蓝色者,才表示亚硝酸过量。
(4)由于临近反应终点,芳伯胺在溶液中的浓度变小,重氮化反应的速度就会变慢,因此,当亚硝酸溶液(或盐酸溶液)加入后,要搅拌3~4min,使亚硝酸尽量与芳伯胺作用,才能检验亚硝酸是否过量。销毁过量亚硝酸的方法是加入少量尿素,直至反应液不再冒出气泡为止。
H2NCONH2+2HNO2—→CO2↑+N2↑+3H2O
9.粗甲基橙为什么要在加热溶解后,再加入固体NaCl进行重结晶?
●答 最初析出的甲基橙颗粒很细,直接抽滤速度很慢,且含杂质过多。先将其加热溶解,再加少量固体NaCl,利用盐析原理使大部分甲基橙更易析出。若让其自然冷却,就可形成较大的结晶,不仅便于抽滤,且杂质较少。
10.在粗甲基橙进行重结晶时,依次用少量水、乙醇和乙醚洗涤,其目的何在?
●答 用水洗涤是为了减少甲基橙吸附的碱。碱性大时,温度稍高,甲基橙就易变质,颜色变深而呈褐色。用少量乙醇、乙醚洗涤,是为了除去剩余的被甲基橙吸附的碱和其他有机物,同时,也是为了使产品甲基橙能迅速变干。湿的甲基橙受光作用后颜色会变深。
11.甲基橙在酸碱溶液中分别呈何种颜色?说明其变色的原因。
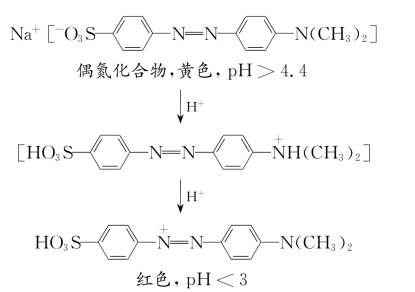
●答 甲基橙是酸碱指示剂中的一种,其变色范围pH值为3.1~4.4。在pH值低于3.1时,溶液呈红色;在pH值大于4.4时,溶液呈黄色。甲基橙的变色原因如下:
12.把冷的重氮盐溶液缓慢倒入低温新制备的CuCl的盐酸溶液中,将会发生什么反应?写出产物的名称。
●答 将会发生桑德迈尔反应,即重氮基被氯取代,同时放出氮气。
![]()
13.N,N 二甲基苯胺与重氮盐偶合时,为什么总是在取代氨基的对位发生?
●答 因为芳环上的取代氨基是个很强的给电子基,通过其与苯环的p-π共轭作用,使苯环的电子云密度增加,尤其是邻对位。由于重氮盐进攻邻位时位阻较大,因此,偶合反应优先发生在取代氨基的对位。当对位被占,则发生在邻位。偶合反应绝对不会在取代氨基的间位上发生。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




