一、实验目的
掌握索氏提取前处理方法原理和基本处理步骤;掌握高效液相色谱分析法中检测器梯度的设置;了解荧光检测器的基本原理及其适用范围;巩固高效液相色谱仪硬件及软件的相关操作;巩固参数设定,数据采集及数据分析的基本要求。
二、实验原理与仪器结构
1.索氏提取
索氏提取(Soxhlet extraction)也是萃取方法的一种,主要是利用溶剂的回流和虹吸原理,对固体混合物中的目标成分进行连续提取。当提取筒中回流下的溶剂的液面超过索氏提取器的虹吸管时,提取筒中的溶剂流回圆底烧瓶内,即发生虹吸。随温度升高,再次回流开始,每次虹吸前,固体物质都能被纯的热溶剂所萃取,溶剂反复利用,缩短了提取时间,所以萃取效率较高。
2.紫外-可见光检测及荧光检测原理
紫外-可见光(VWD)检测原理(略,见实验5.8)。
荧光检测(FLD)原理:许多有机化合物,特别是芳香族化合物、生化物质,被一定强度和波长的紫外光照射后,发射出比激发光波长更长的光,称为荧光。荧光涉及光的吸收和发射两个过程,被化合物吸收的光称为激发光,产生的荧光称为发射光。荧光的性质与分子结构有密切关系,不同结构的分子被激发后,并不是都能发射荧光,但可以与发生荧光的物质反应衍生化后检测。荧光的波长总要长于分子吸收的紫外光波长,通常在可见光范围内。
荧光强度与荧光物质溶液浓度,摩尔吸光系数,吸收池厚度,入射光强度,荧光的量子效率及荧光的收集效率等成正相关,在其他因素保持不变的条件下,物质的荧光强度与该物质溶液浓度成正比,这是荧光检测器的定量基础。当考虑灵敏度时,测定应选择最大激发波长。
荧光检测法最吸引人的特点是它固有的灵敏度和选择性,它的最小检测限往往要比紫外检测法低一个数量级以上。
3.环境中的多环芳烃
多环芳烃(Polycyclic Aromatic Hydro-carbons,PAHs)有机污染物是指两个或两个以上苯环以稠环形式相连的一类化合物。其脂溶性高,不易降解,易在生物体内积累,具有致癌、致畸和致突变的作用,对人类健康和生态环境具有巨大的潜在危害,是全球关注的一类环境污染物。目前,针对环境及食品中的PAHs主流检测方法为HPLC或超高压液相色谱法(UPLC)和GC-MS。在环境监测中,多个国家将HPLC 和GC-MS 列为标准方法。
三、实验条件
1.仪器设备
全自动索氏提取仪(丹麦Foss公司),附带整套工具。
高效液相色谱仪(Agilent HPLC 1200,配稳压电源、四元泵、自动进样器、柱温箱),带荧光检测器和紫外检测器,Agilent Chemstation色谱工作站;PAHs专用色谱柱:Agilent,Zorbax Eclipse,PAH Columns(4.6×100mm×3.5μm)。
旋转蒸发仪,Millipore纯水机,氮吹仪,天平。
2.试剂与样品
16个PAHs化合物标准样品:萘(NaP),苊烯(AcPy),苊(Ace),芴(Flu),菲(PhA),蒽(AnT),荧蒽(FluA),芘(Pyr),苯并[a]蒽(BaA),(Chy),苯并[b]荧蒽(BbF),苯并[k]荧蒽(BkF),苯并[a]芘(BaP),二苯并[a,h]蒽(DbA),苯并[g,h,i]芘(BghiP),茚并[1,2,3-cd]芘(InP)。
甲醇、乙腈、丙酮、环己烷、二氯甲烷、正己烷、正戊烷等为色谱级或农残级试剂;无水硫酸钠,60~200目超纯硅胶,硅藻土,活性铜粉,超纯水。
3.测试参数
进样:进样量为20μL,洗针进样,洗针液为纯乙腈;
泵:流速为1mL/min;流动相为乙腈和水,其梯度洗脱程序见表5-8;运行时间22min,后运行3min;
柱温:25℃;
紫外检测器:检测波长优化后梯度进行,见表5-9;
荧光检测器:检测波长优化后梯度进行,见表5-10。
表5-7 PAH 分析流动相梯度设置

表5-9 PAHs紫外检测波长程序


表5-10 PAHs荧光检测波长程序

四、实验步骤
1.试剂准备
正己烷-丙酮混合液(1∶1):用色谱纯正己烷和丙酮酯按1∶1的体积比混合备用;
正戊烷-二氯甲烷混合液(3∶2):用色谱纯正戊烷和二氯甲烷按3∶2的体积比混合备用;
无水硫酸钠:于马弗炉中420℃温度下烘2h,冷却后备用;
超纯水、乙腈:超声赶气泡。(https://www.xing528.com)
2.样品准备
(1)标准溶液配制
移取适量的混合标准溶液,用甲醇稀释成1μg/mL(以混合标准里浓度最大的标记)混合母液(在4℃下冷藏保存),使用时用甲醇稀释为10~600μg/mL的标准溶液。
(2)样品前处理
准确称取自然风干、研磨过筛(100目)的土壤样品10g,置于具塞玻璃瓶中,加入10g烘好的无水硫酸钠及5g硅藻土,摇匀后转移到索氏提取器的套管中,用80mL配制好的正己烷-丙酮混合液进行自动索氏提取,提取程序:160℃下热浸提60 min,160℃下淋洗60min(EPA 3540C,EPA 3541)。提取液自然冷却后,用20mL环己烷进行溶剂置换,旋转蒸发(65℃)浓缩至1mL左右。参照EPA 3630C 方法,硅胶(配合放置无水硫酸钠和铜粉)柱层析法净化浓缩后的样品。层析柱填充完成后分别用20mL二氯甲烷和正戊烷淋洗,弃去淋洗液,将浓缩后样品提取液加于柱顶部,25mL 正戊烷-二氯甲烷混合液洗脱目标物,收集洗脱液。旋转蒸发浓缩并将洗脱液溶剂置换为甲醇,定容至1mL。样品过0.22μm滤膜,滤液待测。
3.仪器准备
(1)检查流动相,仪器线路,废液瓶等是否准备妥当;
(2)打开电脑,HPLC各组件电源,打开工作软件;
(3)打开工作界面,按操作要求排出所需流动相(乙腈和超纯水)气泡;
(4)配置仪器(配置1100/1200系统模块,选择需要的模块,主要选择需要的检测器),建立平衡柱子的分析方法,保存并运行;
(5)按测试参数设置标准样品分析方法(供参考,可根据仪器及柱型进一步优化)并保存待用。
4.上机分析
(1)待色谱柱平衡后,设置进样程序(sequence),选择标准样品分析方法、设置进样位置、次数等,设置数据保存路径;
(2)运行设置好的标准样品进样程序,开始分析标准系列样品;
(3)得到16个PAHs的色谱图(紫外检测器和荧光色谱图),并对色谱峰进行积分,根据标准样品的浓度和峰面积建立外标曲线,并将其保存到方法中;
(4)按标准样品分析方法,建立未知样品进样程序,分析未知样品,得到样品色谱图;
(5)分析结束后,建立清洗及保存柱子的方法并运行;
(6)所有程序结束后,关泵、关灯,退出程序,关闭主机、电脑及相关附件。
五、实验结果与数据处理
1.实验记录
原始数据记录:记录实验步骤,实验条件,仪器参数,列表记录原始测试结果(标准溶液浓度、信号值以及样品的信号值)。
2.实验结果
(1)参考色谱图(图5-14,图5-15)
(2)PAHs含量计算
利用保留时间定性,外标法定量。注意原始样品经索氏提取后浓度的变化,计算时要考虑称重及最后的浓缩倍数。
六、问题与讨论
1.简述索氏提取技术的进展。
2.分析混合样品时,检测器波长的设置有何要求?
3.HPLC系统压力过高的原因有哪些?
七、注意事项
1.16个PAHs中“苊烯(AcPy)”没有荧光吸收,如果要全部定量,需要辅以紫外检测。
2.在柱层析的装填过程中,注意:①无论是干法装柱还是湿法装柱,都要确保硅胶填料装得紧实以保证层析柱柱效,可以边加边敲打层析柱。②由于溶剂(主要是二氯甲烷)和硅胶之间吸附放热,容易产生气泡,严重时甚至会造成断层,所以要求硅胶一定要填充结实且用稍多溶剂过柱,待柱稳定后再小心上样。

图5-14 PAHs标准样品紫外检测器色谱图
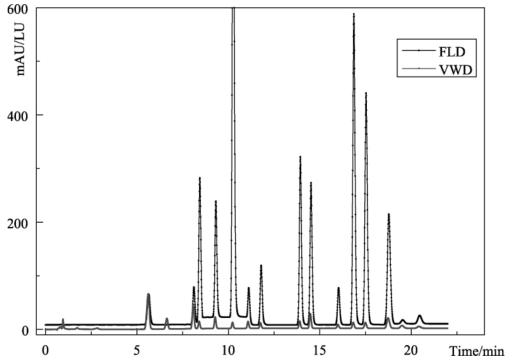
图5-15 PAHs标准样品色谱图——VWD-FLD信号对比
3.在计算样品浓度时,请注意10mg样品经过索氏提取、柱层析净化、旋转蒸发后浓缩至1mL进样,根据外标法计算出浓缩后的样品浓度后,还需要根据浓缩倍数计算出样品实际浓度。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




