4.4.2.1 美拉德反应
分别准确称取5.0±0.05 mg的葡萄糖标准试剂、L-赖氨酸标准试剂和质量比为1︰1的葡萄糖/L-赖氨酸标准试剂混合物,研磨细致并充分混合均匀后放入热重铂坩埚内分别进行热重实验。分析条件为:升温程序为50℃![]() 600℃(保持10 min)。载气为空气,流量200 mL/min。
600℃(保持10 min)。载气为空气,流量200 mL/min。
热重程序升温过程中,样品发生热解,其热解逸出产物的组成和相对含量随温度的升高而不断变化。为了获取样品热解过程中逸出组分的连续变化信息,结合葡萄糖/L-赖氨酸模拟体系非水相美拉德反应热失重图中几个明显的失重段,将整个反应热解过程按每上升50℃(时间约5min)划分为5个温度段连续取样。利用联用装置逐段吸附热解产物,使用5支SPME针头分别对5个温度段的逸出产物进行萃取,并交替使用两套气体取样罐和固相微萃取装置,以便及时清洗取样罐和更换针头。将热重未加样品情况下5min萃取取样获得的结果作为空白对照样。各温度段热解产物吸附完成后,直接将固相微萃取针头插入气相色谱进样口进行脱附,脱附时间为5min。利用GC-MS分析吸附的热解产物。
4.4.2.2 葡萄糖、L-赖氨酸及葡萄糖/L-赖氨酸非水相美拉德反应模拟体系的热学分析
图4-57为葡萄糖在10℃/min升温速率、200 mL/min空气流量条件下热解的热分析曲线。从DTA曲线可以看出,葡萄糖在152℃左右有一个明显的吸热峰,DTA达-65.3 μV,但TG曲线上没有失重,可以推断该峰为葡萄糖的熔融峰。从200℃开始至274℃,葡萄糖发生第一步降解,失重18%,同时分别对应的DTA线和DTG线上都有明显的吸热峰和失重峰,失重速率最大达 378 μg/min。紧接着葡萄糖开始发生第二步降解,从274℃开始到350℃左右,失重率达52%,是葡萄糖热解的主要阶段,同样伴随吸热,DTG出现一个较大的峰,质量损失率最大达1 416 μg/min。450~550℃为葡萄糖热解的快速质量损失过程,同时伴随着剧烈的放热,DTA最大达53.4 μV,550℃时剩余质量仅为原先的3.6%。
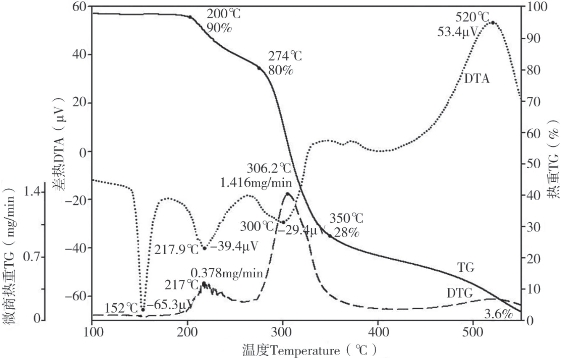
图4-57 葡萄糖热解的热重(TG)、微商热重(DTG)、差热(DTA)-温度(℃)曲线
图4-58为相同条件下L-赖氨酸热解的热分析曲线。TG显示180~250℃为L-赖氨酸第一失重区,失重42.5%,失重速率最大达0.49 mg/min,此温度段降解最快,产生大量挥发性化合物,最大吸热峰同样出现在这个区域,说明L-赖氨酸降解需要吸收大量的热量。根据DTG的两个尖峰,按上式同样的方法计算活化能,得到L-赖氨酸180~210℃、210~250℃受热分解反应的表观活化能分别为484 kJ·mol-1和270 kJ·mol-1。250~500℃为第二失重区。450℃以前DTA显示有一系列的吸热峰,500℃产生一大的放热峰。
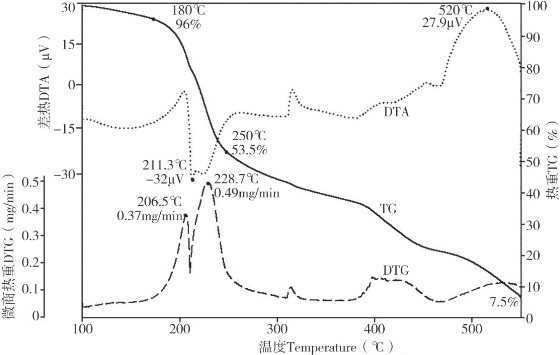
图4-58 L-赖氨酸热解的热重(TG)、微商热重(DTG)、差热(DTA)-温度(℃)曲线
图4-59是葡萄糖和L-赖氨酸按照质量比1︰1混合均匀后的热重(TG)、微商热重(DTG)、差热(DTA)-温度(℃)曲线。葡萄糖与L-赖氨酸混合后熔融峰消失,表明葡萄糖与L-赖氨酸发生了反应。TG曲线表明混合物的第一失重阶段发生在135~245℃,失重40%,最大失重率为326 μg/min,失重的起始温度135℃大大低于葡萄糖和L-赖氨酸各自第一失重点的温度,分别为200℃和180℃。根据DTG曲线上的三个尖峰,按照MUSE软件中的Freeman-Carroll方法计算活化能。135~155℃、155~200℃、200~245℃受热分解反应的表观活化能分别为372 kJ·mol-1、360 kJ·mol-1和358 kJ·mol-1。与葡萄糖、L-赖氨酸各自第一阶段失重对应温度段的降解活化能418.4 kJ·mol-1、484 kJ·mol-1比较也明显偏低。这说明葡萄糖/L-赖氨酸模拟体系非水相美拉德反应的热力学性质比单独的还原糖和氨基酸的热力学性质发生了明显的变化,葡萄糖与L-赖氨酸结合形成美拉德反应的第一步中间产物Amadori化合物后降解在较低的温度点就开始发生了,降解活化能也低于葡萄糖、L-赖氨酸单独降解的活化能。从失重量上比较,葡萄糖第一失重阶段失重18%,与L-赖氨酸混合后第一失重阶段失重高达40%,同时混合物的第一失重阶段伴有一系列的吸热峰,说明此阶段有许多反应发生,产生了较多的挥发性物质。245~355℃为混合物的第二失重阶段,失重较为平缓,DTG维持在60 μg/min左右。355~550℃为第三失重区,伴随着较大的放热峰,峰值达35.4 μV,550℃时剩余质量仅为原先的5.5%。葡萄糖/L-赖氨酸模拟体系的DTA曲线表明,美拉德反应初期为一个吸热过程,反应的发生需要吸收一定的热量,因此反应对温度或固定温度条件下的加热时间有相关性,这和水相中美拉德反应对温度、加热时间有依赖性是一致的。混合物的三步热解期之间没有出现明显的平台,这说明混合物热解失重是一个连续的过程,上一步降解生成中间产物的反应和紧跟着发生中间产物的分解是无法分开的,因此三步降解的起始温度和终止温度及失重情况只是按照失重率的大小做粗略的划分。

图4-59 葡萄糖/L-赖氨酸混合物热解的热重(TG)、微商热重(DTG)、差热(DTA)-温度(℃)曲线
4.4.2.3 针对定向美拉德反应致香产物的条件优化
(1)热解温度段选取
为了揭示葡萄糖/L-赖氨酸模拟体系非水相美拉德反应热解过程中逸出产物的变化情况,针对图4-59的第一和第二热解期,按照温度的连续变化而设计了划分温度段连续取样法,即将样品温度作为每次SPME取样开始和结束的信号。由于热分析仪从50℃开始升温,从混合物TG曲线可以看出50~100℃失重3%左右可能是葡萄糖或L-赖氨酸吸附的部分结晶水,而第二热解期350℃以上为混合物的碳化过程,所以50~100℃、350℃以后的温度段没有进行逸出气体取样。第一、二热解期的温度区间分别为135~245℃和245~355℃。根据混合物的DTG曲线上显示第一热解期出现了3个峰,分别出现在135~155℃、155~200℃、200~245℃3个温度段,每个峰间隔大约为50℃。为了能保证获取最大失重段的逸出气体组分并能满足取样温度的连续性和各温度段热解信息的可比性,在热分析仪10℃/min升温速率条件下,加热至100℃开始进行SPME取样,温度每上升50℃作为一次取样过程,每个温度段的取样时间约为5 min。这样,第一、二热解过程被分为5个温度段,分别为100~150℃、150~200℃、200~250℃、250~300℃、300~350℃。采用划分温度段连续取样方法,通过一次热重试验就可以收集到葡萄糖/L-赖氨酸模拟体系非水相美拉德反应热解过程的逸出产物,之后利用GC/MS进样来分析产物信息。
美拉德反应可以生成许多重要的香味物质,吡嗪类化合物多具有烘烤香,如2-乙基-3,5-二甲基吡嗪、3,5-二乙基-2-甲基吡嗪和2,5-二甲基-3-烯丙基吡嗪具有强烈的巧克力、烤面包、烤坚果的香味;吡咯具有烟草香味;吡啶具有清香;噻唑具有坚果香等。但是由于美拉德反应机理复杂,反应影响因素较多,反应物的种类和配比、反应温度、反应体系含水量、反应时间、pH和压力等均能对反应过程和反应产物造成影响[88]。针对热分析仪程序升温条件下葡萄糖/L-赖氨酸模拟体系非水相美拉德反应,为考察定向致香产物2-乙基-3,5-二甲基吡嗪和3,5-二乙基-2-甲基吡嗪的生成规律,从葡萄糖/L-赖氨酸的配比、热分析仪的升温速率和载气流量三个方面对实验条件进行优化选择。
(2)葡萄糖和L-赖氨酸的配比
分别选取葡萄糖和L-赖氨酸质量比为3︰1,2︰1,1︰1,1︰2,1︰3五种配比进行实验,其对美拉德反应致香产物2-乙基-3,5-二甲基吡嗪和3,5-二乙基-2-甲基吡嗪的总峰面积影响情况如图4-60所示。由图4-60可以看出,葡萄糖和L-赖氨酸质量比为1︰1的总峰面积总体上明显高于其他质量比的峰面积。因此,实验选取质量配比为1︰1进行非水相美拉德反应。

图4-60 葡萄糖/L-赖氨酸不同质量比的美拉德反应致香产物总峰面积比较(https://www.xing528.com)
(3)热分析仪的升温速率和载气流量
在热分析仪中进行葡萄糖/L-赖氨酸非水相美拉德反应,试样的升温是靠热量从经过坩埚再至试样之间的传递进行的。这样,在加热的炉子和试样之间形成了温差。由于混合物试样的物理变化和化学变化引起热焓的变化,试样内部形成了温度梯度,当升温速率增加,这种温差也随之增大[89]。为了避免试样内部温差影响到美拉德反应及造成逸出组分不均衡,热重的升温速率不宜设置得太快。同时,实验使用SPME对热重逸出组分进行萃取吸附,并采用每上升50℃取一次样对整个反应过程划分为5个温度段进行取样。这样热重升温速率就直接关系到逸出组分的取样时间,为了保证SPME合适的萃取时间和满足良好的吸附效果,本实验设定热重升温速率为10℃/min。
热天平周围的气氛对热重法测定有很显著的影响,如果反应是可逆的分解反应,进行热重测定时宜采用静态气氛;而对于复杂不可逆反应,在严格控制实验条件下采用动态气氛,可获得重复性好的实验结果[89]。为了更好地模拟卷烟燃吸期间发生的美拉德反应,实验选择动态空气气氛下进行反应,并分别设定空气流量为100 mL/min、200 mL/min、300 mL/min和400 mL/min进行实验。通过对比不同流量条件下美拉德反应致香产物的总峰面积的变化情况,考察了4种空气流量对定向美拉德反应产物2-乙基-3,5-二甲基吡嗪和3,5-二乙基-2-甲基吡嗪生成的影响,如图4-61所示。由图4-61可以看出,针对两种产物,空气流量设置为200 mL/min的总峰面积明显高于其他流量的总峰面积。

图4-61 葡萄糖/L-赖氨酸混合物不同空气流量下美拉德反应致香产物的总峰面积比较
4.4.2.4 葡萄糖/L-赖氨酸模拟体系非水相美拉德反应热解研究
图4-62为GC-MS获得的逸出产物的总离子流色谱图,图中对比了葡萄糖/L-赖氨酸混合物逸出产物的连续变化情况。图中随温度升高而变化较为明显的色谱峰共有39个,其定性结果列于表4-21中。结合图4-62和表4-21可以看出,反应产物的种类随着温度升高而变化。在较低温度段,产物主要为酮、醚、糠醛等。这是因为葡萄糖和赖氨酸在低温就发生氨基糖的缩合反应,形成的氨基糖经Amadori重排得到的中间产物环化为糠醛类化合物,也可以脱氨形成还原酮或脱氢还原酮。这些酮类在高温阶段又环化和裂解成各种化合物,在此过程中包括了醛醇缩合,醛、氨基聚合以及吡嗪、吡啶、吡咯、噁唑、咪唑等含N杂环化合物的生成。其中二酮类和氨基酸的反应(Strecker降解反应)所生产的醛类和氨基酮是杂环化合物的重要来源[90]。因此,在250~350℃的高温段,大量的杂环化合物被检测到,而且从150℃开始3,5-二羟基-6-甲基-2氢吡喃-4-酮和5-羟甲基糠醛均消失。从图4-62中还可以看出葡萄糖/L-赖氨酸模拟体系非水相美拉德反应在150℃就开始生成致香产物2-乙基-3,5-二甲基吡嗪和3,5-二乙基-2-甲基吡嗪,并且在200~250℃达到最大峰面积,此后的升温反应过程中均能检测出这两种香味产物。
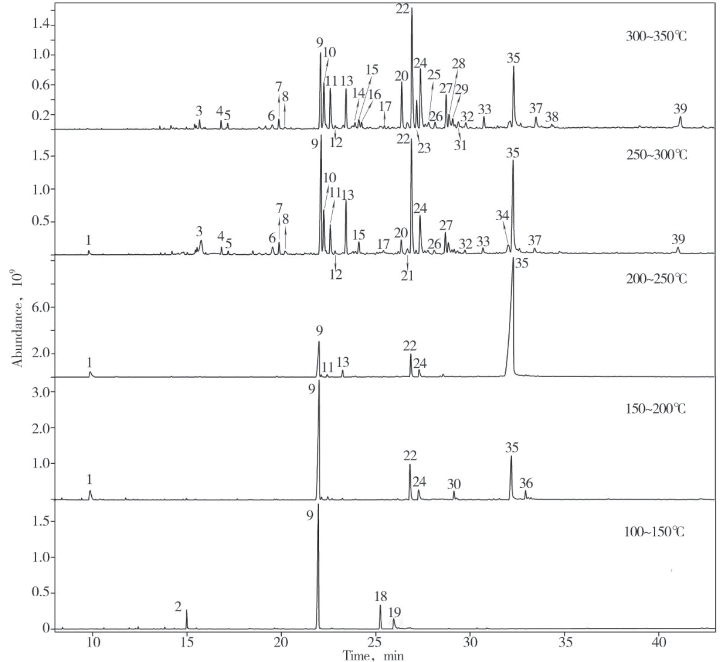
图4-62 葡萄糖/L-赖氨酸混合物不同温度段热解逸出产物的总离子流色谱图对比
表4-21 葡萄糖/L-赖氨酸混合物热解逸出产物的GC-MS分析结果

续表

续表

续表

续表

4.4.2.5 结论
采用热重-固相微萃取-气相色谱-质谱联用研究L-赖氨酸/葡萄糖模拟体系非水相美拉德反应,对反应的热学性质和逸出组分进行表征。结果表明:第一,L-赖氨酸/葡萄糖模拟体系非水相美拉德反应初期为一个吸热过程,反应的发生需要吸收一定的热量,在135~245℃是美拉德反应的第一失重区,大量挥发性香味物质生成。L-赖氨酸/葡萄糖混合物的降解活化能低于L-赖氨酸、葡萄糖单独降解的活化能。第二,针对美拉德反应致香产物2-乙基-3,5-二甲基吡嗪和3,5-二乙基-2-甲基吡嗪设置热分析仪升温速率为10℃/min、空气流量为200 mL/min的条件下能获得最大产量。第三,美拉德反应产物的种类和含量随着温度的变化而变化,低温段生成物以酮类、糠醛类为主,高温段产物主要为吡嗪、吡啶、吡咯、噁唑、咪唑等含N杂环化合物,香味产物2-乙基-3,5-二甲基吡嗪和3,5-二乙基-2-甲基吡嗪自150℃开始生成,200~250℃达最大值。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




