细胞到底是怎样从LDL中摄取胆固醇的?布朗和戈尔茨坦再次回顾了他们之前的研究结果。他们认为,LDL对正常成纤维细胞的“高亲和性”抑制提示细胞表面存在一种高特异性受体分子,只和LDL起作用。他们将这种“细胞表面受体”称为LDL受体。1974年,他们通过125I标记的LDL,在正常成纤维细胞中发现能与之高亲和性结合的LDL受体,而FH成纤维细胞恰恰缺乏这种特异性受体,由此导致了细胞对LDL的摄取障碍。1982年,二人所在实验室从牛的肾上腺中分离提取了LDL受体,并于1984年克隆人LDL受体的cDNA,一年后他们又成功确定了该受体的编码基因。
当然,“细胞表面受体”的理念并非布朗和戈尔茨坦首创。在此之前已有研究证实,细胞表面存在着能够结合激素的相关受体。当时普遍认为,这类受体与细胞表面的配体结合后,能够诱导细胞膜内层的第二信使产生,进而发挥相应的生物学效应。因此,布朗和戈尔茨坦推测,LDL也可能通过此途径发挥作用,即先与其受体结合后再产生某种第二信使,进而抑制HMG-CoA还原酶的活性。
两人的这一推测在他们后来的实验中得到了证实,充当这种第二信使的正是LDL来源的胆固醇,其大致过程是:LDL首先与细胞膜被小凹中的受体结合,形成一种膜被细胞内小泡,并以“内吞”方式进入细胞。之后,膜被小泡中LDL与其受体解离,解离后的受体可回到细胞表面,与LDL再次结合后进行下一轮循环。而解离后的LDL则被溶酶体所吞噬,其中的蛋白质成分降解为氨基酸,而胆固醇则由酸性脂酶水解成一种羟基化衍生物,后者可充当细胞内的第二信使。其既可通过固醇调节元件结合蛋白途径抑制HMG-CoA还原酶的基因转录,又可加速这种蛋白酶的降解,从而抑制HMG-CoA还原酶的活性。上述过程实际上就是布朗和戈尔茨坦后来(1983年)针对LDL摄取过程提出的经典理论——LDL受体介导的内吞作用(图4-3),这一理论同时印证了一个重要理念,即参与代谢的受体是可被循环利用的。LDL受体在细胞内外往返循环一次大约需要10分钟,这样,在其近20小时的生命周期内,该受体可往返循环达数百次。这种高效的受体再循环利用机制,有效地保证了大量的LDL(平均每个LDL颗粒含有1600个胆固醇分子)能被细胞及时摄取并代谢。
而LDL受体这一机制也提示人们,如果能够设法增加受体数量,就能够降低血液中胆固醇水平,不但能够用于治疗FH患者,还很可能对包括冠心病在内的动脉粥样硬化疾病患者有效。所以,布朗和戈尔茨坦发现LDL受体的相关研究成果具有巨大的基础理论意义,对心脏病的预防和治疗产生了深远的影响。因此,被认为是人类探索体内胆固醇代谢机制的一座里程碑。(https://www.xing528.com)
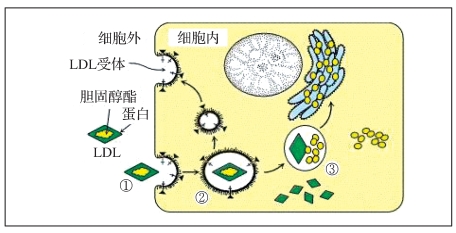
图4-3 低密度脂蛋白受体介导的低密度脂蛋白内吞过程
主要分为三步:①血液中LDL与细胞膜上受体结合;②结合受体的LDL被内吞进入细胞内;③LDL被细胞内的溶酶体水解(降解)
布朗和戈尔茨坦现仍担任德克萨斯大学医学中心西南医学院分子遗传学系资深评议教授。许多著名的大学和研究机构曾试图诱导他们离开德克萨斯大学,但均未成功。两人的贡献没有高低大小之分,因为几乎每篇论文都是两人共同署名。这两位学者的友情恰似LDL与其受体的特异性结合,并以“合体”的形式绽放出绚丽的智慧之光,为科研人员的协作关系树立了伟大榜样,值得中国科学界学习!
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




