前面叙述了酶催化反应机制及影响酶反应的环境因素,但没有涉及底物浓度和酶浓度对酶催化反应速度的影响以及反应速度(速率)的定量描述,即酶反应动力学问题。无论是酶反应还是非酶反应,其反应速度除受到反应物和催化剂浓度影响外,还同时受到与活化能相关的内在动力学因素的影响。由于不同反应条件下反应物的浓度可能不同,因此采用基于内在因素的反应动力学常数来比较不同催化剂的相对催化活力才更有意义。如果已知某一环境条件下的反应速度常数,那么就可以预测该条件下任意一组反应物和催化剂浓度下的反应速度。
1902年Henri在研究蔗糖酶催化水解蔗糖的反应时得到如图6-19所示的反应速度(V)与底物浓度([S])的“双曲线”形关系曲线。当底物浓度较低时,反应速度与底物浓度呈线性关系,之后随着底物浓度的增加,反应速度不是呈直线增加,继续加大底物浓度,反应速度趋向一个极限,表明酶已被底物饱和。这种现象在非酶催化反应中则是不存在的。
图6-19 蔗糖浓度对转化酶活力的影响
(一)米氏动力学
1913年Michaelis和Menten根据中间产物学说对“双曲线”反应图形加以数学推导,提出了所谓的快速平衡假定,即快速平衡模型:
式中 E—游离状态酶;
ES—酶-底物络合物;
k 1、k-1—各个反应的速度常数。
这个方程式的运算基于以下三个假说:
(1)测定的速度为反应初速度,底物浓度[S]消耗很少,仅占[S]原始浓度的5%以内,故在测定反应速度所需的时间内,产物P的生成极少,(E+P)的逆转可以忽略不计。
(2)底物浓度[S]大大地高于酶的浓度[E],因此[ES]的形成不会明显地降低底物浓度[S]。
(3)ES解离成(E+S)的速度也大大超过ES分解形成(P+E)的速度,即k-1远远大于k2或者E+S ES的可逆反应在测定初始速度υ的时间内已达到动态平衡,而少量P的生成不影响这个平衡,故称为快速平衡假定。
ES的可逆反应在测定初始速度υ的时间内已达到动态平衡,而少量P的生成不影响这个平衡,故称为快速平衡假定。
一般说来,底物总是大大过量,上述这些假设符合实际情况。另外,如果仅测定反应的初速度,此时[P]接近于0。ES分解形成(P+E)这一步是整个反应的限制步骤。
由于E和ES处于平衡,因此可以写出一个平衡式(6-4),再经重排得到式(6-6)。
假设ES形成E+S的解离常数为Km,因此:
若E的原始浓度为[E]0,在反应平衡时,E的浓度变为([E]0-[ES]),而此时根据上述假定⑵,S的浓度[S]保持不变。故(6-6)式变为:
由于反应速度v取决于[ES],即v=k2[ES]
当[S]为极大时,全部E转变为ES,[ES]=[E]0,此时v=vmax(最大反应速度),故vmax=k2[E]0
将式(6-10)和式(6-11)代入式(6-9),可得
式(6-12)即为根据平衡假定推导出的米氏方程(Michaelis-Menten方程),式中Km称为米氏常数,即ES的解离常数。
如果将式(6-13)移项整理可得:
由于vmax和Km均为常数,而v和[S]为变量,故式(6-16)实际上可写成(x-a)(y+b)=k。该式实质上为典型的双曲线方程,可见米氏方程与试验结果是相符的。
当Km≥[S]时,即底物浓度很小时,则式(6-13)中的Km+[S]≈Km,此时式(6-13)可写成:
此时,反应对底物为一级反应,其速度与[S]呈正比。
当Km远远小于[S]时,则式(6-12)的分母中的Km可以忽略,式(6-13)可以写成:
此时,反应速度达到最大的恒定值,反应速度与底物的浓度无关,该化学反应属零级反应。
当 ,代入式(6-13)可得
,代入式(6-13)可得
由式(6-20)可知,米氏常数Km值是当反应的初速度为v为最大反应速度vmax的一半时的底物浓度,单位为mol/L。
米氏常数是酶学研究中的一个极为重要的常数。
(1)Km是酶的特征常数之一,一般只与酶的性质有关,而与酶浓度无关。
(2)如果一个酶有几种底物,则每一种底物对应一个特定的Km值,Km与pH和温度有关。因此,Km只是在pH、温度和其他条件一定时才有意义。对一定底物的常数而言,条件改变或底物改变,Km也会随之发生改变。
(3)1/Km可近似地表示酶对底物亲和力的大小。Km愈小,表明酶与底物的亲和力愈大,说明ES不易解离成(E+S),而E和S很容易结合形成ES。同一种酶有几种底物时,其中Km最小的底物一般称为该酶的最适底物或天然底物。
(二)酶反应动力学常数测定
对感兴趣的酶而言,vmax(与k2成比例)和Km的确定是极为重要的,这两项的确定可以使我们对一定酶和底物浓度条件下酶催化反应速度的快速程度进行预测。式(6-21)是米氏方程的积分形式,它对了解和控制食品加工中的酶反应非常有用。
式中,[S]0是底物起始浓度,[S]是t时刻的底物浓度。得到预期的底物转化分数X(X=([S]0-[S])/[S]0)的时间为
该关系可以为在规定时间内反应达到期望程度必须添加多少酶([E]0=vmax/k2)提供合理估计。不过,该等式仅提供粗略估算,因为可以导致酶反应背离预期进程的原因有很多,例如共反应物/底物的损耗、产物抑制、酶的逐渐失活、反应条件变化等。
1.Lineweaver-Burk法
将米氏方程两边取倒数,即有:
式(6-23)为Lineweaver-Burk方程。根据该方程, 对
对 作图得到一条直线,斜率为Km/vmax,纵坐标截距为1/vmax,横坐标截距为-1/Km,如图6-20所示。
作图得到一条直线,斜率为Km/vmax,纵坐标截距为1/vmax,横坐标截距为-1/Km,如图6-20所示。
为提高vmax和Km值的测定精确度,一般将[S]定在0.2Km~0.5Km范围。表6-8所示为求酵母菌脱羧酶催化的反应的Km值及vmax值测得的数据,作图得图6-21。由图6-21可知,1/Km为20L/mol,1/vmax为0.125min/(mol/L)。进一步计算得Km=0.05mol/L,vmax=80mol/(L·min)。
表6-8 酵母菌脱羧酶反应速度
图6-20 Lineweaver-Burk作图法求Km与vmax
图6-21 Lineweaver-Burk作图法求酵母菌脱羧酶的Km与vmax
2.Eadie-Hofstee法
将米氏方程移项整理后可得:
故
v对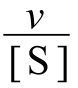 作图可得一条直线(图6-22),纵坐标轴截距为vmax,横坐标截距为
作图可得一条直线(图6-22),纵坐标轴截距为vmax,横坐标截距为 。(https://www.xing528.com)
。(https://www.xing528.com)
图6-22 Eadie-Hofstee作图法Km与vmax
(三)底物的抑制与激活作用
当底物浓度过高时,反应速度会随着浓度的进一步增加而下降。这是因为:①反应物浓度过高时,反应体系中分子的扩散和运动会受到抑制;②过量的底物和酶的激活剂结合,激活剂的有效浓度下降;③过量的底物分子与酶分子作用,有可能生成无活性的中间产物,而且这个中间产物不能分解成反应产物。
不过,有时当底物浓度较高时,反应速度随底物浓度上升的速度比Michaelis-Menten的计算值还要高,即高浓度的底物会激活反应。这可解释为:一个底物分子结合至酶的活性部位导致正常的产物形成,第二个底物分子结合在酶的另一个部位不会导致底物分子转变成产物,但是它能提高在活性部位结合的底物分子转变成产物的速度。
(四)变构动力学性质
变构性质的定义是v-[S]关系为一条S形曲线,而符合Michaelis-Menten性质的v-[S]关系则是一条双曲线。当[S]<<Km时,增加[S]对v的影响比预期的小,而当[S]处在Km附近时,[S]对v的影响比预期的大,这就是正变构动力学性质。而在某些情况下,当[S]较低时,[S]对v的影响比预期的要大,然后,v并没有随[S]的增加而提高很多,这是负的变构动力学性质。
为了区分变构性质和Michaelis-Menten性质,Koshland等提出了一个用以测量协同作用的方程式:
式中[S]0.9和[S]0.1分别是v0=0.9vmax和v0=0.1vmax时的底物浓度。
对于所有具有Michaelis-Menten性质的酶Rs是81,而具有正变构性质的酶Rs<81(往往低于30~40),对于具有负变构性质的酶Rs>81。
具有变构性质的酶通常为多亚基酶。Koshland等认为,对于具有变构性质的酶,两个或更多个亚基必须显示协同作用。如果第二个底物分子比第一个底物分子更容易(更牢固)与酶结合,这时表现为正变构性质。如果第一个底物分子比第二个底物分子更牢固地与酶结合,这时表现为负变构性质。如果两底物分子与酶的结合情况相同,彼此间对与酶的结合没有影响,此时表现为Michaelis-Menten性质。
对于具有变构性质的酶,在Km附近,底物浓度对酶反应速度的影响特别大。在糖酵解和三羰酸循环中的代谢酶往往显示变构性质。对于某些酶,非底物化合物也能引起变构性质,它们起到了变构抑制剂或激活剂的作用。
如前所述,有些物质能抑制甚至阻止酶催化反应的进行。这种作用称为酶的抑制作用,这种物质称为抑制剂。抑制作用有不可逆性抑制和可逆性抑制。不可逆抑制剂一旦与酶结合,酶的催化活力永久性丧失。可逆抑制不同于不可逆抑制,区别在于:
(1)可逆抑制剂快速地(在几个毫秒内)与酶形成非共价扩散控制平衡络合物,通过透析或凝胶过滤色谱可使此平衡络合物离解和酶活力复原;
(2)不可逆抑制剂缓慢地与酶形成酶的共价衍生物,不能通过透析或凝胶过滤使后者离解。
根据抑制剂对Lineweaver-Burk图的斜率、vmax、Km或变构效应的影响,可以鉴别四类可逆抑制剂,即:竞争性抑制剂、非竞争性抑制剂、反竞争性抑制剂和变构抑制剂。Lineweaver-Burk方程在存在抑制剂和不存在抑制剂时的差别仅表现在斜率和/或截距上。
(一)竞争性抑制
在竞争性抑制中,底物和竞争抑制剂竞争与酶相结合,如式(6-28)所示。
式中,I和EI分别为抑制剂和酶-抑制剂络合物,[I]和[EI]分别为游离状态抑制剂的浓度和酶-抑制剂络合物浓度。KEI为酶-抑制剂络合物EI的离解常数。
EI不能与S结合,也不能形成一个产物。[E]0为酶的初始浓度,因此
将式(6-29)和式(6-30)应用到Michaelis-Menten方程推导中,得到
式中v是存在抑制剂时的酶反应的初速度;Km为不存在抑制剂时的米氏常数;vmax为不存在抑制剂时的最大反应速度。因此可以得到存在可逆抑制剂时的Lineweaver-Burk方程为
在竞争性抑制中,米氏常数加(1+[I]/KEI)倍,但vmax不变,如图6-23所示。
图6-23 竞争性抑制剂对Lineweaver-Burk图的影响
(二)非竞争性抑制
对于此类抑制作用,抑制剂没有和底物竞争与酶结合,因此抑制剂和底物能同时与酶结合,存在如下平衡:
式中,ESI为酶-底物-抑制剂络合物,[ESI]为酶-底物-抑制剂络合物浓度。KESI为酶-底物-抑制剂络合物ESI的离解常数。
如果假设KESI=KEI,ESI不能转变成产物,则可得到简单的线性非竞争性抑制的Michaelis-Menten方程的形式:
相应的Lineweaver-Burk方程为
在简单的线性非竞争性抑制作用中,Y-截距和斜率都改变了(1+[I]0/Ki)倍,如图6-24所示。
图6-24 非竞争性(简单线性)抑制剂对Lineweaver-Burk图的影响
(三)反竞争性抑制
不同于竞争性和非竞争性抑制,在反竞争性抑制中抑制剂不能和游离酶结合,仅能和一个或几个中间络合物结合。
此时的Michaelis-Menten方程式的适当形式:
相应的Lineweaver-Burk和转换式:
存在反竞争性抑制作用与不存在抑制作用相比,Y-截距改变了1+[I]0/KESI倍,但斜率不变,如图6-25所示。
图6-25 反竞争抑制剂对Lineweaver-Burk图的影响
(四)变构抑制作用
变构抑制作用通常是由抑制剂与多亚基酶结合而造成的。如前文所描述底物结合时的变构性质那样,当第二个底物分子比第一个底物分子更容易(更牢固)与酶结合时,表现为正变构性质;当第一个底物分子比第二个底物分子更牢固地与酶结合,表现为负变构性质。如果两底物分子与酶的结合情况相同,彼此间对与酶的结合没有影响,则表现为Michaelis-Menten性质。
(五)消化酶抑制剂
1.脂肪酶抑制剂
脂肪酶抑制剂是一类能够特异性抑制人体胃和肠道内脂肪酶活性的物质,主要来源于化学合成、天然植物提取物和微生物代谢产物,其化学本质与作用机理因其来源不同而有所差异。活性较强且研究较清楚的脂肪酶抑制剂是含β-内酯环的天然产物。脂肪酶抑制剂可有效抑制胃和肠道中脂肪酶对脂肪的分解催化作用,从而达到减少脂肪吸收、控制和治疗肥胖的目的。水皂角、葡萄、橄榄和鼠尾草等植物中有较高含量的脂肪酶抑制剂,如水皂角中的黄烷二聚物等。链霉菌是生产脂肪酶抑制剂的主要微生物。1987年,瑞士罗氏公司从Streptomyces toxytricini中找到有效脂肪酶抑制剂lipstatin。lipstatin是一种强效的胰脂肪酶不可逆抑制剂,含有N-甲酰-L-亮氨酸链,其四氢衍生物orlistat性质更稳定,可减少饮食中30%脂肪的吸收,于1997年被FDA批准为抗肥胖药。
2.α-淀粉酶抑制剂
α-淀粉酶抑制剂是一类能够特异性抑制人体唾液和肠道α-淀粉酶的物质,广泛存在于豆类、谷类、水果、昆虫和微生物代谢产物中,其中,白芸豆含有较多的α-淀粉酶抑制剂,而且生物安全性也较高。α-淀粉酶抑制剂的化学本质因来源不同而有所差异,主要有含氮碳水化合物、多肽和蛋白质三种类型。目前,从白芸豆中提取的α-淀粉酶抑制剂是相对分子质量为56000的糖蛋白,亚基组成为α2β2,通过与α-淀粉酶按摩尔比1∶1形成复合物而发挥抑制作用,其抑制类型为非竞争性抑制。从白芸豆中提取的α-淀粉酶抑制剂已被广泛地用于控制和治疗糖尿病、肥胖等由糖代谢紊乱引起的疾病。
3.蛋白酶抑制剂
蛋白酶抑制剂是一类能与蛋白酶活性部位或变构部位结合来抑制蛋白酶的催化活性或阻止蛋白酶原转化为有活性蛋白酶的小分子质量的多肽或蛋白质,广泛存在于动植物和微生物体内,在豆科、茄科、葫芦科、禾本科及十字花科等草本植物中存在较多,而在木本植物中较少。按其所作用的蛋白酶活性部位的不同,蛋白酶抑制剂可分为丝氨酸蛋白酶抑制剂、半胱氨酸蛋白酶抑制剂、金属羧肽酶蛋白酶抑制剂和天冬氨酸蛋白酶抑制剂。在众多蛋白酶抑制剂中,大豆胰蛋白酶抑制剂的研究最为广泛。
大豆胰蛋白酶抑制剂属于丝氨酸蛋白酶抑制剂,是由72~197个氨基酸残基组成的多肽。大豆胰蛋白酶抑制剂有7~10种,根据其氨基酸组成、相对分子质量、等电点、与不同蛋白酶的结合力以及免疫学的反应性等特点,可将其分为两大类:①Kunitz胰蛋白酶抑制剂,相对分子质量为20000~25000,呈易变的非螺旋形,对热不稳定,含有两对二硫键,能特异抑制胰蛋白酶。一个抑制剂分子可以结合一分子的胰蛋白酶。其在大豆中含量约为1.4%;②Bowman-Birk胰蛋白酶抑制剂,相对分子质量为6000~10000,含有较多二硫键,具有热稳定性,能对胰蛋白酶、胰凝乳蛋白酶及弹性蛋白酶发生特异性抑制。一个抑制剂分子可以结合两个分子的胰蛋白酶。其在大豆中的含量约为0.6%。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




