抗原与抗体的结合反应是一切免疫测定技术的最基本原理。在此基础上结合一些生化或理化方法作为信号显示或放大系统即可建立免疫测定法,如放射免疫测定法、酶免疫测定法、荧光免疫测定法等。人们一直在不断寻找新的显示方法应用于免疫检测技术,其方法学研究和实际应用十分活跃。
一个成功的免疫测定法必备三个要素:性能优良的抗体、灵敏和专一性的标记物和高效的分离手段。
抗原与抗体的结合反应是依靠局部(抗原决定簇和抗体结合位点)的分子间作用力结合的。其作用力主要有:氢键、范德华力、盐键、疏水相互作用。形成稳定的作用力要求抗体结合位点和抗原决定簇的空间结构高度互补,而且其接触表面基团分布要两相配合。
现有的主要免疫测定法如表5-1所示。按照是否使用标记物分为标记免疫测定法和非标记免疫测定法,后者又称为经典免疫测定法;按反应介质分为均相或非均相(免疫复合物需分离后检测)免疫测定法;按反应状态分为平衡态或非平衡态免疫测定法。按照标记物种类,标记免疫测定法又分为放射性标记测定法和非放射性标记测定法。
表5-1 免疫测定方法分类
经典免疫测定法灵敏度较低,在残留分析中极少应用。放射性标记测定法因辐射污染和试剂寿命等问题已逐渐淘汰。非放射性免疫测定法种类繁多,发展较快,包括各种酶免疫测定法、荧光免疫测定法、化学发光免疫测定法、脂质体免疫测定法等。非均相方法需要免疫复合物分离步骤,适用范围广泛;均相方法不需要分离,易实现自动化,但灵敏度不如非均相方法,标记物易受样品基质的影响,适用范围小。
(一)ELISA的基本原理
ELISA(Enzyme-Linked immunosorbent assay)的基础是抗原或抗体的固相化及抗原或抗体的酶标记。这一方法的基本原理是:①使抗原或抗体结合到某种固相载体表面,并保持其免疫活性。②使抗原或抗体与某种酶连接成酶标抗原或抗体,这种酶标抗原或抗体既保留其免疫活性,又保留酶的活力。在测定时,把受检标本(测定其中的抗体或抗原)和酶标抗原或抗体按不同的步骤与固相载体表面的抗原或抗体起反应。用洗涤的方法使固相载体上形成的抗原抗体复合物与其他物质分开,最后结合在固相载体上的酶量与标本中受检物质的量成一定的比例。加入酶反应的底物后,底物被酶催化变为有色产物,产物的量与标本中受检物质的量直接相关,所以可根据颜色反应的深浅定性或定量分析。由于酶的催化速率很高,所以可极大地放大反应效果,从而使测定方法达到很高的敏感度。
(二)ELISA的类型
ELISA可用于测定抗原,也可用于测定抗体。在这种测定方法中有三个必要的试剂:①固相的抗原或抗体,即“免疫吸附剂”(immunosorbent);②酶标记的抗原或抗体,称为“结合物”(conjugate);③酶反应的底物。
根据试剂的来源和标本的情况以及检测的具体条件,可设计出各种不同类型的检测方法。用于检验的ELISA主要有以下几种类型:
1.双抗体夹心法测抗原
双抗体夹心法是检测抗原最常用的方法,操作步骤如图5-1所示:
图5-1 双抗夹心ELISA法原理图
(1)将特异性抗体与固相载体联结,形成固相抗体 洗涤除去未结合的抗体及杂质。
(2)加受检标本,保温反应 标本中的抗原与固相抗体结合,形成固相抗原抗体复合物。洗涤除去其他未结合物质。
(3)加酶标抗体,保温反应 固相免疫复合物上的抗原与酶标抗体结合。彻底洗涤未结合的酶标抗体。此时固相载体上带有的酶量与标本中受检抗原的量相关。
(4)加底物显色 固相上的酶催化底物成为有色产物。通过比色,测得标本中抗原的量。在检验中,此法适用于检验各种蛋白质等大分子抗原。只要获得针对受检抗原的特异性抗体,就可用于包被固相载体和制备酶结合物而建立此法。如抗体的来源为抗血清,包被和酶标用的抗体最好分别取自不同种属的动物。如应用单克隆抗体,一般选择两个针对抗原上不同决定簇的单抗,分别用于包被固相载体和制备酶结合物。这种双位点夹心法具有很高的特异性,而且可以将受检标本和酶标抗体一起保温反应,作一步检测。
2.双抗原夹心法测抗体
反应模式与双抗体夹心法类似。用特异性抗原进行包被和制备酶结合物,以检测相应的抗体。与间接法测抗体的不同之处为以酶标抗原代替酶标抗抗体。此法中受检标本不需稀释,可直接用于测定,因此其敏感度相对高于间接法。本法关键在于酶标抗原的制备,应根据抗原结构的不同,寻找合适的标记方法。
3.间接法测抗体
间接法是检测抗体常用的方法。其原理为利用酶标记的抗抗体(抗人免疫球蛋白抗体)以检测与固相抗原结合的受检抗体,所以称为间接法,如图5-2所示。操作步骤如下:
图5-2 间接ELISA法测抗体原理图
(1)将特异性抗原与固相载体联结,形成固相抗原 洗涤除去未结合的抗原及杂质。
(2)加稀释的受检血清,保温反应 血清中的特异抗体与固相抗原结合,形成固相抗原抗体复合物。经洗涤后,固相载体上只留下特异性抗体,血清中的其他成分在洗涤过程中被洗去。
(3)加酶标抗体 可用酶标抗人Ig以检测总抗体,但一般多用酶标抗人IgG检测IgG抗体。固相免疫复合物中的抗体与酶标抗抗体结合,从而间接地标记上酶。洗涤后,固相载体上的酶量与标本中受检抗体的量正相关。
(4)加底物显色 间接法的优点是只要变换包被抗原就可利用同一酶标抗抗体建立检测相应抗体的方法。间接法成功的关键在于抗原的纯度。虽然有时用粗提抗原包被也能取得实际有效的结果,但应尽可能予以纯化,以提高试验的特异性。间接法中一种干扰因素为正常血清中所含的高浓度的非特异性。血清中受检的特异性IgG只占总IgG中的一小部分。IgG的吸附性很强,非特异IgG可直接吸附到固相载体上,有时也可吸附到包被抗原的表面。因此在间接法中,抗原包被后一般用无关蛋白质(例如,牛血清蛋白)再包被一次,以封闭(blocking)固相上的空余间隙。另外,在检测过程中标本须先行稀释(1∶40~1∶200),以避免过高的阴性本底影响结果的判断。
4.竞争法测抗体
当抗原材料中的干扰物质不易除去,或不易得到足够的纯化抗原时,可用此法检测特异性抗体。其原理为标本中的抗体和一定量的酶标抗体竞争与固相抗原结合。标本中抗体量越多,结合在固相上的酶标抗体越少,因此阳性反应呈色浅于阴性反应。如抗原为高纯度的,可直接包被固相。如抗原中会有干扰物质,直接包被不易成功,可采用捕获包被法,即先包被与固相抗原相应的抗体,然后加入抗原,形成固相抗原。洗涤除去抗原中的杂质,然后与固相抗原竞争结合。另一种模式为将标本与抗原一起加入到固相抗体中进行竞争结合,洗涤后再加入酶标抗体,与结合在固相上的抗原反应,如图5-3所示。
图5-3 竞争ELISA法测抗体原理图
5.竞争法测抗原
小分子抗原或半抗原因缺乏可作夹心法的两个以上的位点,因此不能用双抗体夹心法进行测定,可以采用竞争法模式。其原理是标本中的抗原和一定量的酶标抗原竞争与固相抗体结合。标本中抗原量含量越多,结合在固相上的酶标抗原越少,最后的显色也越浅。小分子激素、药物等ELISA测定多用此法。
(三)ELISA的材料与试剂
完整的ELISA试剂盒包含以下各组分:
(1)已包被抗原或抗体的固相载体(免疫吸附剂)。
(2)酶标记的抗原或抗体(结合物)。
(3)酶的底物。
(4)阴性对照品和阳性对照品(定性测定中),参考标准品和控制血清(定量测定中)。
(5)结合物及标本的稀释液。
(6)洗涤液。
(7)酶反应终止液。
1.免疫吸附剂
已包被抗原或抗体的固相载体在低温(2~8℃)干燥的条件下一般可保存6个月。有些不完整的试剂盒,仅供应包被用抗原或抗体,检测人员需自行包被。下文简述固相载体和包被过程。
(1)固相载体 固相载体在ELISA测定过程中作为吸附剂和容器,不参与化学反应。可作ELISA中载体的材料很多,最常用的是聚苯乙烯。聚苯乙烯具有较强的吸附蛋白质的性能,抗体或蛋白质抗原吸附其上后仍保留原来的免疫学活性,加之它的价格低廉,所以被普遍采用。聚苯乙烯为塑料,可制成各种形式。
ELISA载体的形状主要有三种:微量滴定板、小珠和小试管。以微量滴定板最为常用,专用于EILSA的产品称为ELISA板,国际上标准的微量滴定板为8×12的96孔式。为便于作少量标本的检测,有制成8联孔条或12联孔条的,放入座架后,大小与标准ELISA板相同。ELISA板的特点是可以同时进行大量标本的检测,并可在特制的比色计上迅速读出结果。现在已有多种自动化仪器用于微量滴定板型的ELISA检测,包括加样、洗涤、保温、比色等步骤,对操作的标准化极为有利。
良好的ELISA板应该是吸附性能好,空白值低,孔底透明度高,各板之间、同一板各孔之间性能相近。聚苯乙烯ELISA板由于原料的不同和制作工艺的差别,各种产品的质量差异很大,因此,每一批号的ELISA板在使用前须事先检查其性能。
(2)包被的方式 将抗原或抗体固定在固相载体表面的过程称为包被(coating)。换言之,包被即是抗原或抗体结合到固相载体表面的过程。蛋白质与聚苯乙烯固相载体是通过物理吸附结合的,靠的是蛋白质分子结构上的疏水基团与固相载体表面的疏水基团间的作用。这种物理吸附是非特异性的,受蛋白质的分子质量、等电点、浓度等的影响。载体对不同蛋白质的吸附能力是不相同的,大分子蛋白质较小分子蛋白质通常含有更多的疏水基团,所以更易吸附到固相载体表面。IgG对聚苯乙烯等固相具有较强的吸附力,其联结多发生在Fc段上,抗体结合点暴露于外,因此抗体的包被一般均采用直接吸附法。蛋白质抗原大多也可采用与抗体相似的方法包被。
(3)包被用抗原 用于包被固相载体的抗原按其来源不同可分为天然抗原、重组抗原和合成多肽抗原三大类。天然抗原可取自动物组织、微生物培养物等,须经提取纯化才能作包被用。重组抗原是抗原基因在质粒体中表达的蛋白质抗原,多以大肠杆菌或酵母菌为质粒体。重组抗原的优点是除工程菌成分外,其他杂质少,而且无传染性,但纯化技术难度较大。重组抗原的另一特点是能用基因工程制备某些无法从天然材料中分离的抗原物质。合成多肽抗原是根据蛋白质抗原分子的某一抗原决定簇的氨基酸序列人工合成的多肽片段。多肽抗原一般只含有一个抗原决定簇,纯度高,特异性也高,但由于分子质量太小,往往难于直接吸附于固相上。多肽抗原的包被一般需先使其与无关蛋白质,如牛血清白蛋白质(BSA)等偶联,借助于偶联物与固相载体的吸附,间接地结合到固相载体表面。
(4)包被用抗体 包被固相载体的抗体应具有高亲和力和高特异性,可取材于抗血清或含单克隆抗体的腹水或培养液。如免疫用抗原中含有杂质(即便是极微量的),在抗血清中将出现杂抗体,必须除去(可用吸收法)后才能用于ELISA,以保证试验的特异性。抗血清不能直接用于包被,应先提取IgG,通常采用硫酸铵盐析和SepHadex凝胶过滤法。一般经硫酸铵盐析粗提的IgG已可用于包被,高度纯化的IgG性质不稳定。如需用高亲和力的抗体包被以提高试验的敏感性,则可采用亲和层析法以除去抗血清中含量较多的非特异性IgG。腹水中单抗的浓度较高,特异性也较强,因此不需要作吸收和亲和层析处理,一般可将腹水作适当稀释后直接包被,必要时也可用纯化的IgG。应用单抗包被时应注意,一种单抗仅针对一种抗原决定簇,在某些情况下,用多种单抗混合包被,可取得更好的效果。
(5)包被的条件 包被用抗原或抗体的浓度,包被的温度和时间,包被液的pH等应根据试验的特点和材料的性质而选定。抗体和蛋白质抗原一般采用pH9.6的碳酸盐缓冲液作为稀释液,也有用pH7.2的磷酸盐缓冲液及pH7~8的Tris-HCl缓冲液作为稀释液。通常在ELISA板孔中加入包被液后,在4~8℃冰箱中放置过夜,37℃中保温2h被认为具有同等的包被效果。包被的最适当浓度随载体和包被物的性质可有很大的变化,每批材料需通过实验与酶结合物的浓度协调选定。一般蛋白质的包被浓度为100ng/mL~20μg/mL。
(6)封闭 封闭(blocking)是继包被之后用高浓度的无关蛋白质溶液再包被的过程。抗原或抗体包被时所用的浓度较低,吸收后固相载体表面尚有未被占据的空隙,封闭就是让大量不相关的蛋白质充填这些空隙,从而排斥在ELISA其后的步骤中干扰物质的再吸附。封闭的手续与包被相类似。最常用的封闭剂是0.05%~0.5%的牛血清白蛋白,也有用10%的小牛血清或1%明胶作为封闭剂的。脱脂奶粉也是一种良好的封闭剂,其最大的特点是价廉,可以高浓度(5%)使用。高质量的速溶食用低脂乳粉即可直接当作封闭剂使用,但由于乳粉的成分复杂,而且封闭后的载体不易长期保存,因此在试剂盒的制备中较少应用。
2.结合物
结合物即酶标记的抗体(或抗原),是ELISA中最关键的试剂。良好的结合物应该是既保有酶的催化活力,也保持了抗体(或抗原)的免疫活性。结合物中酶与抗体(或抗原)之间有恰当的分子比例,在结合试剂中应尽量不含有或少含有游离的(未结合的)酶或游离的抗体(或抗原)。此外,结合物尚要有良好的稳定性。
(1)酶 用于ELISA的酶应符合以下要求:纯度高,催化反应的转化率高,专一性强,性质稳定,来源丰富,价格不贵,制备成酶结合物后仍继续保留它的活力部分和催化能力。最好在受检标本中不存在相同的酶。另外,它的相应底物易于制备和保存,价格低廉,有色产物易于测定等。在ELISA中,常用的酶为辣根过氧化物酶(horseradish peroxidase,HRP)和碱性磷酸酶(alkaline phosohatase,AP)。
(2)抗原和抗体 制备结合物时所用的抗体一般为纯度较高的IgG,以免在与酶联结时受到其他杂蛋白的干扰。最好用亲和层析纯的抗体,这样全部酶结合物均具有特异的免疫活性,可以在高稀释度进行反应,实验结果本底浅淡。在ELISA中用酶标抗原的模式不多,总的要求是抗原必须是高纯度的。
(3)结合物的制备 酶标记抗体的制备方法主要有两种,即戊二醛交联法和过碘酸盐氧化法。
①戊二醛交联法:戊二醛是一种双功能团试剂,它可以使酶与蛋白质的氨基通过它而联结。碱性磷酸一般用此法进行标记。交联方法有一步法、两步法两种。在一步法中戊二醛直接加入酶与抗体的混合物中,反应后即得酶标记抗体。ELISA中常用的酶一般都用此法交联。它具有操作简便、有效(结合率达60%~70%)和重复性好等优点。缺点是交联反应是随机的,酶与抗体交联时分子间的比例不严格,结合物的大小也不均一,酶与酶,抗体与抗体之间也有可能交联,影响效果。在两步法中,先将酶与戊二醛作用,透析除去多余的戊二醛后,再与抗体作用而形成酶标抗体。也可先将抗体与戊二醛作用,再与酶联结。两步法的产物中绝大部分的酶与蛋白质是以1∶1的比例结合的,较一步法的酶结合物更有助于本底的改善以提高敏感度,但其偶联的有效率较一步法低。
②过碘酸盐氧化法:本法只适用于含糖量较高的酶。辣根过氧化物酶的标记常用此法。反应时,过碘酸钠将HRP分子表面的多糖氧化为醛基很活泼,可与蛋白质上的氨基形成Schiff氏碱而结合。酶标记物按摩尔比例联结,其最佳比例为:酶/抗体=(1~2)/1。此法简便有效,一般认为是HRP最可取的标记方法,但也有人认为所用试剂较为强烈,各批实验结果不易重演。
按以上方法制备的酶结合物一般都混有未结合物的酶和抗体。理论上,结合物中混有的游离酶一般不影响ELISA中最后的酶活力测定,因经过彻底洗涤,游离酶可被除去,并不影响最终的显色。但游离的抗体则不同,它会与酶标抗体竞争相应的固相抗原,从而减少了结合到固相上的酶标抗体的量。因此制备的酶结合物应予纯化,去除游离的酶和抗体后用于检测,效果更好。纯化的方法很多,分离大分子化合物的方法均可应用。硫酸铵盐析法最为简便,但效果并不理想,因为此法只能去除留在上清中的游离酶,但相当数量的游离抗体仍与酶结合物一起沉淀而不能分开。用离子交换层析或分子筛分离更为可取,高效液相层析法可将制备的结合物清晰地分成三个部分:游离酶、游离抗体和纯结合物而取得最佳的分离效果,但费用较高。
结合物制得后,在用作ELISA试剂前尚需确定其适当的工作浓度。使用过浓的结合物,既不经济,又使本底增高;结合物的浓度过低,则又影响检测的敏感性。所以必须对结合物的浓度予以选择。最适的工作浓度就是指结合物稀释至这一浓度时,能维护一个低的本底,并获得测定的最佳灵敏度,得到最合适的测定条件和节省测定费用。就酶标抗体本身而言,它的有效工作浓度是指与其相应抗原包被的载体作试验时,能得到阳性反应的最高稀释度。
(4)结合物的保存 酶标抗体中的酶和抗体均为生物活性物质,保存不当,极易失活。高浓度的结合物较为稳定,冷冻干燥后可在普通冰箱中保存一年左右,但冻干过程中引起活力的降低,而且使用时需经复溶,颇为不便。结合物溶液中加入等体积的甘油可在低温冰箱或普通冰箱的冰格中较长时间保存。早期的ELISA试剂盒中的结合物一般均按以上两种形式供应,配以稀释液,临用时按标明的稀释度稀释成工作液。现在较先进的ELISA试剂盒均已用合适的缓冲液配成工作液,使用时不需再行稀释,在4~8℃保存期可达6个月。由于蛋白质浓度较低,结合物易失活,需加入蛋白保护剂。另外再加入抗生素(例如庆大霉素)和防腐剂(HRP结合物加硫柳泵,AP结合物可加叠氮钠),以防止细菌生长。
(5)结合物的稀释液 用于稀释高浓度的结合物以配成工作液。为避免结合物在反应中直接吸附在固相载体上,在稀释缓冲液中常加入高浓度的无关蛋白质(例如1%牛血清白蛋白),通过竞争以抑制结合物的吸附。一般还加入具有抑制蛋白质吸附于塑料表面的非离子型表面活性剂,如吐温20,0.05%的浓度较为适宜。在间接测定抗体时,血清标本需稀释后进行测定,也可应用这种稀释液。
3.酶的底物
(1)HRP的底物 HRP催化过氧化物的氧化反应,最具代表性的过氧化物为H2O2,其反应式如下:
DH2+H2O2→ D+2H2O
上式中,DH2为供氧体,H2O2为受氢体。在ELISA中,DH2一般为无色化合物,经酶作用后成为有色的产物,以便作比色测定。常用的供氢体有邻苯二胺(O-phenylenedia-mine,OPD)和四甲基联苯胺(3,3′,5,5′-tetramethylbenzidine,TMB)。
OPD氧化后的产物呈橙红色,用酸终止酶反应后,在492nm波长处有最高吸收峰,灵敏度高,比色方便,是HRP结合物最常用的底物。OPD本身难溶于水,OPD·2HCl为水溶性。曾有报道OPD有致突变性,操作时应予注意。OPD见光易变质,与过氧化氢混合成底物应用液后更不稳定,须现配现用。在试剂盒中,OPD和H2O2一般分成两个组分,OPD可制成一定量的粉剂或片剂形式,片剂中含有发泡助溶剂,使用更为方便。过氧化氢则配入底物缓冲液中,制成易保存的浓缩液,使用时用蒸馏水稀释。先进的ELISA试剂盒中则直接配成含保护剂的工作浓度为0.02% H2O2的应用液,只需加入OPD后即可作为底物应用液。
TMB经HRP作用后其产物显蓝色,目视对比鲜明。TMB性质较稳定,可配成溶液试剂,只需与H2O2溶液混合即成应用液,可直接作底物使用。另外,TMB又有无致癌性等优点,因此在ELISA中应用日趋广泛。酶反应用HCl或H2SO4终止后,TMB产物由蓝色变为黄色,可在比色计中定量,最适吸收波长为405nm。
(2)AP的底物 AP为磷酸酯酶,一般采用对硝基苯磷酸酯(p-nitrophenyl phosphate,p-NPP)作为底物,可制成片剂,使用方便。产物为黄色的对硝基酚,在405nm波长处有吸收峰。用NaOH终止酶反应后,黄色可稳定一段时间。
AP也有发荧光底物(磷酸4-甲基伞酮),可用于ELISA作荧光测定,敏感度较高于用显色底物的比色法。
4.稀释液
洗板式ELISA中,常用的稀释液为含0.05%吐温20的磷酸缓冲盐水。
5.酶反应终止液
常用的HRP反应终止液为硫酸,其浓度按加量及比色液的最终体积而异,在板式ELISA中一般采用2mol/L。
6.阳性对照品和阴性对照品
阳性对照品(positive control)和阴性对照品(negative control)是检验试验有效性的控制品,同时也作为判断结果的对照,因此对照品,特别是阳性对照品的基本组成应尽量与检测标本的组成相一致。
7.参考标准品
定量测定的ELISA试剂盒应含有制作标准曲线用的参考标准品,应包括覆盖可检测范围的4~5个浓度,一般均配入含蛋白保护剂及防腐剂的缓冲液中。
(四)ELISA的操作和注意事项
1.加样
在ELISA中一般有3次加样步骤,即加标本,加酶结合物,加底物。加样时应将所加物加在LEISA板孔的底部,避免加在孔壁上部,并注意不可溅出,不可产生气泡。加标本一般用微量加样器,按规定的量加入板孔中。每次加标本应更换吸嘴,以免发生交叉污染。如此测定(如间接法ELISA)需用稀释的血清,可在试管中按规定的稀释度稀释后再加样。也可在板孔中加入稀释液,再在其中加入血清标本,然后在微型振荡器上振荡1min以保证混合。加酶结合物应用液和底物应用液时可用定量多道加液器,使加液过程迅速完成。
2.保温
在ELISA中一般有两次抗原抗体反应,即加标本和加酶结合物后。抗原抗体反应的完成需要有一定的温度和时间,这一保温过程称为温育(incubation)。温育常采用的温度有43℃、37℃、室温和4℃(冰箱温度)等。37℃是实验室中常用的保温温度,也是大多数抗原抗体结合的合适温度。在建立ELISA方法作反应动力学研究时,实验表明,两次抗原抗体反应一般在37℃经1~2h,产物的生成可达顶峰。保温的方式除有的ELISA仪器附有特制的电热块外,一般均采用水浴。
3.洗涤
洗涤在ELISA过程中虽不是一个反应步骤,但却也决定着实验的成败。ELISA就是靠洗涤来达到分离游离的和结合的酶标记物的目的。通过洗涤以清除残留在板孔中没能与固相抗原或抗体结合的物质,以及在反应过程中非特异性地吸附于固相载体的干扰物质。现在多采用洗板机程序洗涤。
4.显色和比色
显色是ELISA中的最后一步温育反应,此时酶催化无色的底物生成有色的产物。反应的温度和时间仍是影响显色的因素。在定量测定中,加入底物后的反应温度和时间应按规定力求准确。
OPD底物显色一般在室温或37℃反应20~30min后即不再加深,再延长反应时间,可使本底值增高。TMB受光照的影响不大,经HRP作用后,约40min显色达顶峰,随即逐渐减弱,至2h后即可完全消退至无色。TMB的终止液有多种,叠氮钠和十二烷基硫酸钠(SDS)等酶抑制剂均可使反应终止。
酶标比色仪简称酶标仪,通常指专用于测读ELISA结果吸光度的光度计。酶标仪的主要性能指标有:测读速度、读数的准确性、重复性、精确度和可测范围、线性等。优良的酶标仪的读数一般可精确到0.001,准确性为±1%,重复性达0.5%。普通的酶标仪A值在0.000~2.900,甚至更高。超出可测上限的A值常以“*”或“over”或其他符号表示。应注意可测范围与线性范围的不同,线性范围常小于可测范围,比如某一酶标仪的可测范围为0.000~2.900,而其线性范围仅0.000~2.000,这在定量ELISA中制作标准曲线时应予注意。测读A值时,要选用产物的敏感吸收峰,如OPD用492nm波长。也可用双波长式测读,即每孔先后测读两次,第一次在最适波长(W1),第二次在不敏感波长(W2),两次测定间不移动ELISA板的位置。例如,OPD用492nm波长为W1,630nm波长为W2,最终测得的A值为两者之差(W1-W2)。双波长式测读可减少由容器上的划痕或指印等造成的光干扰。
5.结果判断
(1)定性测定 定性测定的结果判断是对受检标本中是否含有待测抗原或抗体作出“阳性”“阴性”表示。“阳性”表示该标本在该测定系统中有反应,“阴性”则为无反应。在间接法和夹心法ELISA中,阳性孔呈色深于阴性孔。在竞争法ELISA中则相反,阴性孔呈色深于阳性孔。两类反应的结果判断方法不同,分述于下。
①间接法和夹心法:这类反应的定性结果可以用肉眼判断。目视标本无色或近于无色者判为阴性,显色清晰者为阳性。但在ELISA中,正常人血清反应后常可出现呈色的本底,此本底的深浅因试剂的组成和实验的条件不同而异,因此实验中必须加测阴性对照。阴性对照的组成应为不含受检物的正常血清或类似物。在用肉眼判断结果时,更宜用显色深于阴性对照作为标本阳性的指标。
目视法简捷明了,但颇具主观性。在条件许可下,应该用比色计测定吸光值,这样可以得到客观的数据。先读出标本(S)、阳性对照(P)和阴性对照(N)的吸光值,然后进行计算。计算方法有多种,大致可分为阳性判定值法和标本与阴性对照比值法两类。
a.阳性判定值:阳性判定值一般为阴性对照A值加上一个特定的常数,以此作为判断结果阳性或阴性的标准。用此法判断结果要求实验条件十分恒定,试剂的制备必须标准化,阳性和阴性的对照品应符合一定的规格,须配用精密的仪器,并严格按规定操作。阳性判定值公式中的常数是在这特定的系统中通过对大量标本的实验检测而得到的。现举某种检测HBsAg的试剂盒为例。试剂盒中的阴性对照品为不含HBsAg的复钙人血浆,阳性对照品HBsAg的含量标明为P=(9±2)ng/mL。每次试验设2个阳性对照和3个阴性对照。测得A值后,先计算阴性对照A值的平均数(NCX)和阳性对照A值的平均数(PCX),两个平均数的差(PCX-NCX)必须大于一个特定的数值(例0.400),试验才有效。3个阴性对照A值均应≥0.5×NCX,并≤1.5×NCX,如其中之一超出此范围,则弃去,而另两个阴性对照重新计算NCX;如有两个阴性对照A值超出以上范围,则该次实验无效。阳性判定值按下式计算:
标本A值>阳性判定值的为阳性,小于阳性判定值的为阴性。应注意的是,式中0.05为该试剂盒的常数,只适合于该特定条件下,而不是对各种试剂均可通用。根据以上叙述可以看出,在这种方法中阴性对照和阳性对照也起到试验的质控作用,试剂变质和操作不当均会产生“试验无效”的后果。
b.标本/阴性对照比值:在实验条件(包括试剂)较难保证恒定的情况下,这种判断法较为合适。在得出标本(S)和阴性对照(N)的A值后,计算S/N值。在早期的间接法ELISA中,有些作者定出S/N为阳性标准,现多为各种测定所沿用。实际上每一测定系统应该用实验求出各自的S/N的阈值。有的试剂盒中所设阴性对照为不含蛋白质或蛋白质含量较低的缓冲液,以致反应后产生的本底可能较正常人血清的本底低得多。因此,这类试剂盒,如N<0.05(或其他数值),则按0.05计算,否则将出现假阳性结果。
②竞争法:在竞争法ELISA中,阴性孔呈色深于阳性孔。阴性呈色的强度取决于反应中酶结合物的浓度和加入竞争抑制物的量,一般调节阴性对照的吸光度在1.0~1.5之间,此时反应最为敏感。
竞争法ELISA不易用自视判断结果,因肉眼很难辨别弱阳性反应与阴性对照的显色差异,一般均用比色计测定,读出S、P和N的吸光值。计算方法主要也有两种,即阳性判定值法和抑制率法。
a.阳性判定值法:与间接法和夹心法中的阳性判定值法基本相同,但在计算公式中引入阳性对照A值,现举某种检测抗HBc的试剂盒为例。试剂盒中的阴性对照为不含抗HBc的复钙人血浆,阳性对照中抗HBc含量为(125±100)μ/mL。每次试验设2个阳性对照和3个阴性对照。测得A值后,先计算阴性对照A值的平均值(NCX)和阳性对照A值的平均数(PCX),两个平均数的差(NCX-PCX)必须大于一个特定的数值(例如0.300),试验才有效。3个阴性对照A值均应小于2.000,而且应≥0.5×NCX,并≤1.5×NCX,如其中之一超出此范围,则弃去,而以另2个阴性对照重新计算×NCX;如有2个阴性对照A值超出以上范围,则该次实验无效。阳性判定值按下式计算:
标本A值≤阳性判定值的反应为阳性,A值>阳性判定值的反应为阴性。
b.抑制率法:抑制率表示标本在竞争结合中标本对阴性反应显色的抑制程度,按下式计算:
一般规定抑制率≥50%为阳性,<50%为阴性。
(2)定量测定ELISA操作步骤复杂,影响反应因素较多,特别是固相载体的包被难达到各个体之间的一致,因此在定量测定中,每批测试均须用一系列不同浓度的参考标准品在相同的条件下制作标准曲线。测定大分子质量物质的夹心法ELISA,标准曲线的范围一般较宽,曲线最高点的吸光度可接近2.0,绘制时常用半对数纸,以检测物的浓度为横坐标,以吸光度为纵坐标,将各浓度的值逐点连接,所得曲线一般呈S形,其头、尾部曲线趋于平坦,中央较呈直线的部分是最理想的检测区域。测定小分子质量物质常用竞争法,其标准曲线中吸光度与受检物质的浓度呈负相关。标准曲线的形状因试剂盒所用模式的差别而略有不同。ELISA测定的标准曲线中横坐标为对数关系,这更有利于测定系统的表达。
(一)人工完全抗原的合成
1.试剂与材料
①SM2:磺胺二甲基嘧啶(Sulfamethazine,SMT)。
②BSA:牛血清白蛋白(Bovine Serum Albumen)。
③OVA:卵清白蛋白(Ovalbumin)。
④SA:丁二酸酐(Succinic anhydride)。
⑤EDC·HCl:1-乙基-3(3-二甲基氨基丙基)-碳二亚胺·盐酸盐。
⑥无水吡啶(Pyridine)。
⑦无水处理的二氯甲烷(CH2Cl2)。
2.实验方法
(1)半抗原SM2-SA的制备SM2-SA合成的方程式如图5-4所示。
①取1.405g SM2溶于10mL无水处理过的吡啶。
②2.67g SA溶于5mL无水吡啶,与SM2液混匀溶解。
③搅拌反应24h。
④反应液移入置有20mL水的100mL分液漏斗中摇匀静置。
⑤用15mL CH2Cl2进行萃取,轻摇,注意放气。萃取3次,收集下层CH2Cl2相。
⑥合并3次萃取CH2Cl2相。用0.1mol/L HCl溶液15mL洗提,3次后用15mL H2O再洗一次。收集下层CH2Cl2相。
⑦在萃取液中加入一定量的无水Na2SO4脱水。
⑧在蒸发皿中加入2mL甲苯,低温(35℃)蒸干。
图5-4 SM2-SA合成方案方程式图
(2)琥珀酰化-水溶性碳化二亚胺法合成SM2-BSA、SM2-OVA(水溶性EDC法)
①称取BSA和OVA各200mg、100mg SM2-SA和100mg EDC中分别溶于5、2、3mL的PBS中。
②然后向BSA和OVA溶液中边搅拌边慢慢滴加2mL SM2-SA溶液和2mL EDC溶液。在4℃冰浴下遮光反应4h。
再向混合液中滴加剩下的1mL EDC溶液。继续于4℃冰浴下遮光搅拌反应24h。
③反应结束后4000r/min离心5min,取上清液装入透析袋,用0.01mol/L pH7.4 PBS在4℃透析2d(PBS:1.5mmol/L KH2PO4,8mmol/L Na2HPO4,2.7mmol/L KCl,137mmol/L NaCl),每天更换3次透析液。
④透析完毕后上sepHadex G-50层析柱,用100mmol/L pH7.4 PBS洗提,留小部分鉴定,其余用冷冻干燥机干燥后分装。
合成路线如图5-5所示。
(二)合成抗原的鉴定
抗原合成结果进行SDS-PAGE分析和紫外光谱分析,并计算结合比测定。
(三)抗体的制备与纯化
1.兔免疫
第一次免疫取100μg合成抗原与1mL弗氏完全佐剂(FCA)乳化的抗原(FCA-IgG)液,背部皮下散点注射各0.2mL左右。第二次免疫在3周后用弗氏不完全佐剂乳化注射。第三次、第四次免疫同第二次免疫方法,间隔为2周。抗血清效价达到要求以后采血。
2.抗体纯化
图5-5 琥珀酰化—水溶性碳化二亚胺法合成SM2-BSA方程式图
按饱和硫酸铵法和DEAE纤维素法进行。
3.结果鉴定
以双相琼脂扩散试验定性观察检测所获免疫血清的抗体质量,以直接竞争法确定抗血清效价。
(四)标准竞争抑制曲线的制作
1.包被微孔板
用乙醇-PBS(0.15mol/L,pH7.2)400倍稀释的SM2-OVA人工抗原包被酶标板,150μL/孔,4℃过夜。
2.稀释
将纯化抗体稀释80倍后分别与等量不同浓度的SM2标准溶液用2mL试管混合振荡,使SM2的最终浓度为10μg/mL、1μg/mL、500ng/mL、100ng/mL、50ng/mL、10ng/mL、5ng/mL、1ng/mL、0.5ng/mL、0.1ng/mL,分别加100μL/孔,4℃静置。
3.洗涤
取出酶标板恢复至室温,弃去包被液,每孔加300μL洗涤液,静置3min,弃去洗涤液,共洗3次,在吸水纸上将酶标板敲干。
4.封闭
加封闭液封闭,250μL/孔,置37℃下温育1h。
5.抗原抗体反应
酶标板洗3×3min后,加抗体抗原反应液(在酶标板的适当孔位加抗体稀释液作为阴性对照,3孔;加抗原稀释液作为阳性对照,3孔)130μL/孔,37℃,温育2h。
6.酶标记反应
倒掉反应液并拍干,酶标板洗3×3min,拍干,加酶标二抗-羊抗兔HRP结合物(1∶200,V/V)100μL/孔,37℃下1h。
7.测定
酶标板用洗液洗5×3min。加底物溶液A、B,各100μL/孔,37℃,温育15min,然后加终止液,40μL/孔,以终止显色反应,酶标仪450nm/630nm测出OD值。
8.作图(https://www.xing528.com)
求出各孔的B校正值:B校正值=OD实测值-空白对照孔OD值(均值)。
求出标准样的B/B0值:B=[B校正值/阴性对照孔B0校正值(均值)]×100。
以标准样浓度对数值为横坐标,B/B0的均值为纵坐标作图。
(五)畜产品中SM2残留的ELISA检测
屠宰现场取肝、肾、肌肉、血各100g。放入清洁保鲜袋内,加封,标明标记,保温冷藏及时送实验室。将试样分别放入高速组织捣碎机中捣碎,充分混匀,装入清洁的容器内,加封后,标明标记。应于-18℃冷冻保存。
1.样品预处理
样品处理:称取肉(肝、肾)均质后的样品20g置入250mL长颈瓶中,加入甲醇∶水为80∶20的溶液200mL。摇匀后在70℃水浴中加热45min。在摇床上振荡60min。1500r/min离心10min。用巴斯德吸管吸去脂肪层,取上清液低温蒸干后用含有0.0032%BSA的10mL乙酸溶液(pH7.0,10mmol/L)溶解。
2.IC-ELISA程序
(1)包被微孔板 用400倍稀释的SM2-OVA人工抗原包被酶标板,150μL/孔,4℃过夜。
(2)将纯化抗体SM2-BSA稀释80倍后分别与等量样品提取液(10倍稀释)用2mL试管混合振荡后,4℃静置(15min左右)。
(3)洗涤 取出酶标板恢复至室温,弃去包被液,每孔加300μL洗涤液,静置3min,弃去洗涤液,共洗3次,在吸水纸上将酶标板敲干。
(4)封闭 加封闭液(1%的BSA)封闭,250μL/孔(200),置37℃下温育1h。
(5)抗原抗体反应 酶标板洗3×3min后,加抗体抗原反应液(如表2-4所示,在酶标板的适当孔位加抗体稀释液作为阴性对照,3孔;加抗原稀释液作为阳性对照,3孔)130μL/孔,37℃,温育2h。
(6)酶标记反应 倒掉反应液并拍干,酶标板洗3×3min,拍干,加酶标二抗-羊抗兔HRP结合物(1∶200,V/V)100μL/孔,37℃下1h。
(7)测定 酶标板用洗液洗5×3min。加底物溶液A、B,各100μL/孔,37℃,温育15min,然后加终止液,40μL/孔,以终止显色反应,酶标仪450nm/630nm测出OD值。
(8)计算 求出各孔的B校正值:B校正值=OD实测值-空白对照孔OD值(均值)。
求出标准样的B/B0值:B=[B校正值/阴性对照孔B0校正值(均值)]×100。
对照标准曲线拟合方程,求出待测样SM2含量(ng/mL)。
(六)方法评价
1.特异性
特异性是指本测定方法对被测物质的专一程度,一般用抗体交叉反应表示。该方法假定100%的被测抗原可与50%的抗体结合,那么可与50%的抗体结合的被测抗原类似物百分含量则为抗体与该类似物的交叉反应率(CR50%)。计算公式如下:
式中 S——标准抗原的IC50;
Z——抗原类似物与50%的抗体结合时的浓度。
2.灵敏度
本实验灵敏度即指应用该方法能检出待测物中SM2残留的最低含量,即最小检出量(LOD)。测定10个“0”标准管,求出光密度值的平均数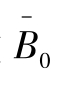 ,减去三倍的标准差
,减去三倍的标准差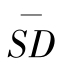 再与
再与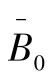 的比值。对照标准曲线方程得出浓度值即为检测限值。
的比值。对照标准曲线方程得出浓度值即为检测限值。
抗原浓度对数与吸光度值有较好线性关系的一段浓度值可以作为工作检测范围。测量限(LOQ)是指实际操作中半定量检测SM2的最小测定量,通常被定为“0”管光密度值平均数的80%。
3.准确度
取有代表性的高中低三个浓度为目标浓度添加至空白猪血清中,混匀后进行IC-ELISA试验计算回收率。
4.精确度
批内误差:以标准缺陷的批内变异系数表示:
CV=SD的平均值/平均批内平均结合率×100(%)
批间误差:以3次测定的结合率进行平均,求出各浓度的批间变异系数,再平均求其总的批间变异系数。
(一)实验原理
采用间接竞争ELISA方法,在微孔条上包被偶联抗原,试样中残留的阿维菌素类药物与酶标板上的偶联抗原竞争阿维菌素抗体,加入酶标记的抗体后,显色剂显色,终止液终止反应。用酶标仪在450nm处测定吸光度,吸光值与阿维菌素类药物残留量呈负相关,与标准曲线比较即可得出阿维菌素类药物残留含量。
(二)试剂和材料
1.阿维菌素类药物试剂盒
(1)96孔板(12条×8孔)包被有阿维菌素偶联抗原。
(2)阿维菌素标准溶液(至少有5个倍比稀释浓度水平,外加1个空白)。
(3)阿维菌素抗体溶液。
(4)过氧化物酶标记物。
(5)底物显色溶液A液 过氧化尿素。
(6)底物显色溶液B液 四甲基联苯胺。
(7)反应终止液1mol/L硫酸。
(8)缓冲液(2倍浓缩液)。
(9)洗涤液(20倍浓缩液)。
2.乙腈、正己烷、无水硫酸钠(分析纯)。
3.碱性氧化铝柱Sep-Pak Vac 12cc(2g)。
4.水
GB/T 6682规定的一级水。
5.缓冲液工作液
用水将2倍的浓缩缓冲液按1∶1体积比进行稀释(1份2倍浓缩缓冲液+1份水),用于溶解干燥的残留物,缓冲液工作液在4℃可保存一个月。
6.洗涤液工作液
用水将20倍的浓缩洗涤液按1∶19体积比进行稀释(1份20倍浓缩洗涤液+19份水),用于酶标板的洗涤,洗涤工作液在4℃可保存一个月。
(三)仪器
1.酶标仪(配备450nm滤光片)。
2.超声波清洗器。
3.离心机。
4.氮气吹干仪。
5.匀浆机。
6.振荡器。
7.涡旋式混合器。
8.微量移液器(单道20、50、100μL,多道50~300μL可调)。
(四)试样制备与保存
取新鲜或解冻的动物组织,剪碎,10000r/min匀浆1min。-20℃下保存。
(五)试样测定
1.提取
称取牛肉、牛肝试样(3.0±0.05)g于50mL聚苯乙烯离心管中,加9mL乙腈、3mL正己烷,置于振荡器上振荡10min,加3g无水硫酸钠,再振荡10min,3000r/min以上、15℃离心10min,去除上层正己烷,取下层4.0mL提取液备用。
称取3g无水硫酸钠平铺在碱性氧化铝柱 Sep-PakVac上,加10mL乙腈洗柱,再加4.0mL提取液,开始收集滤液,待提取液流干后,再加入4mL乙腈清洗柱子,合并洗液和滤液至10mL干净的玻璃试管中,于50~60℃水浴氮气流下吹干。
取1.0mL缓冲液工作液溶解干燥的残留物,涡动1min,超声10min,涡动1min,取溶解后的样品液100μL,加入100μL缓冲液工作液,充分混合,取20μL用于分析。
2.测定
使用前将试剂盒在室温(19~25℃)下放置1~2h。
(1)将标准和试样(至少按双平行实验计算)所有数量的孔条插入微孔架,记录标准和试样的位置。
(2)加20μL系列标准溶液或处理好的试样溶液到各自的微孔中。标准和试样至少做两个平行试验。
(3)加抗体工作液80μL到每一个微孔中,充分混合,于37℃恒温箱中孵育30min。
(4)倒出孔中液体,将微孔架倒置在吸水纸上拍打以保证完全除去孔中的液体。用250μL洗涤液工作液充入孔中,再次倒掉微孔中液体,再重复操作两遍以上(或用洗板机洗涤)。
(5)加100μL过氧化物酶标记物,37℃恒温箱中孵育30min。
(6)倒出孔中液体,将微孔架倒置在吸水纸上拍打以保证完全除去孔中的液体。用250μL洗涤液工作液充入孔中,再次倒掉微孔中液体,再重复操作两遍以上(或用洗板机洗涤)。
(7)加50μL底物显色液A液和50μL底物显色液B液,混合并在37℃恒温箱避光显色15~30min。
(8)加50μL反应终止液,轻轻振荡混匀,用酶标仪在450nm处测量吸光度值。
(六)结果计算
用所获得的标准溶液和试样溶液吸光度值与空白溶液吸光度值的比值进行计算,见式(5-5):
式中 Ar——相对吸光度值,%;
B——标准(试样)溶液的吸光度值;
B0——空白(浓度为0的标准溶液)的吸光度值。
将计算的相对吸光度值(%)对应阿维菌素(μg/L)的自然对数作半对数坐标系统曲线图,对应的试样浓度可从校正曲线算出,见式(5-6):
式中 X——试样中阿维菌素类的含量,μg/kg;
ρ——试样的相对吸光度值(%)对应的阿维菌素类含量,g/L;
f——试样稀释倍数;
m——试样的取样量,g。
计算结果保留到小数点后两位。阳性结果应用确证法确证。
(七)交叉反应
阿维菌素:100%;埃普利诺菌素:130%;伊维菌素:33%;多拉菌素:5%;泰乐菌素:<0.1%;替米考星:<0.1%。
(八)精密度
本方法的批内变异系数<30%,批间变异系数<45%。
(一)适用范围
本方法适用于转基因大豆及其初级加工产品中CP4 EPSPS蛋白的检测,也适用于含有CP4 EPSPS蛋白的其他转基因植物检测。
(二)实验原理
酶标板表面包被有特异的单克隆捕获抗体。当加上测试样品时,捕获抗体与抗原特异性结合,未结合的样品成分通过洗涤除去。洗涤之后,加入与辣根过氧化物酶偶联的多克隆抗体,该抗体可与CP4 EPSPS蛋白的另一个抗原表位特异结合,洗涤之后,加入辣根过氧化物酶的显色底物四甲基联苯胺。HRP可催化底物产生颜色反应,颜色信号与抗原浓度在一定范围内呈线性关系。显色一定时间后,加入终止液终止反应。在450nm波长测每一孔的光密度。
(三)试剂
1.检测试剂盒通常提供的试剂
(1)大豆抽提缓冲液 硼酸钠缓冲液,pH7.5。
(2)大豆分析缓冲液 磷酸盐缓冲液,Tween-20,BSA,pH7.4。
(3)包被有单克隆捕获抗体的酶标孔。
(4)与辣根过氧化物酶偶联的兔抗。
(5)偶联抗体稀释剂10%热灭活的小鼠血清。
(6)显色底物。
(7)终止液0.5%硫酸。
(8)10倍浓缩的洗涤缓冲液 PBS,Tween-20,pH7.1。
(9)与基质匹配的阴性和阳性标准品,如0.1%,0.5%,1%,2%,5%。
2.其他需要准备的试剂
(1)70%的甲醇溶液(体积比)取700mL甲醇加水定容至1000mL。
(2)95%的乙醇。
(四)仪器设备
1.通常实验室仪器设备。
2.酶标仪;多通道移液器。
3.孔径450μm的滤膜;孔径150μm的滤膜。
(五)操作步骤
1.样品的预处理
取500g以上大豆,粉碎、微孔滤膜过滤。在操作过程中小心避免污染,避免局部过热。定性检测的微孔滤膜孔径应为450μm,保证孔径小于450μm的粉末质量占大豆样品质量的90%以上。定量检测的样品先用孔径为450μm的微孔滤膜过滤后,再经孔径为150μm的微孔滤膜过滤,过滤得到的样品量只要能满足检测要求即可。对于其他类型的材料采用类似的方法处理。
在检测不同批次样品之间应将处理大豆样品的所有设备进行彻底清洁。首先,尽可能除去残留材料,然后用酒精洗涤两遍,用水彻底清洗,风干。同时,工作区应保持清洁,避免样品交叉污染。
2.样品抽提
测试样品、阴性及阳性标准品在相同条件下抽提两次。每一种标准品在称量时按照含量由低到高的顺序进行。
将每一种样品称出(0.5±0.01)g,放入15mL聚丙烯离心管中。为避免污染,在称量不同样品时,用酒精棉擦干净药匙并晾干,或使用一次性药匙。向每个离心管中加4.5mL抽提缓冲液。将缓冲液与管内物质剧烈混匀并涡旋振荡,使之成为均一的混合物(低脂粉末和分离蛋白质需延长混合时间,有时超过15min;全脂粉末容易混匀,不超过5min)。4℃下5000×g离心15min。小心吸取上清液于另一干净的聚丙烯离心管中,每管吸取1mL上清液。上清液可于2~8℃贮存,时间不超过24h。
在检测前,用大豆检测缓冲液按比例稀释样品溶液,如表5-2所示。
表5-2 不同墓质的稀释度
3.ELISA操作步骤
ELISA实验流程如表5-3所示。
表5-3 ELISA实验流程
续表
(1)孵育 在室温下,取出酶标板,加10μL稀释的样品溶液及对照到酶标孔中,轻轻混匀。37℃孵育1h(每次加样应该更换一次性吸头,以免交叉污染。并使用胶带或铝箔封住酶标板,以免交叉污染和蒸发)。
(2)洗涤 把10倍浓缩的洗涤缓冲液用水稀释10倍,用洗涤工作液洗涤酶标板3次。在此过程中,不要让酶标孔干,否则会影响分析结果;不管是人工洗涤还是自动洗涤,应确保每一孔用相同体积的洗液洗涤,以免出现错误的结果。
人工洗涤:将酶标板翻转,倒出微孔内液体。用装有洗涤工作液的500mL洗瓶,将每孔注满洗涤液,保持60s,然后翻转,倒掉洗涤液。如此重复操作总共3次。在多层纸巾上将酶标板倒拍数次,以去除残液(用胶带将酶标板条固定以免滑落)。
自动洗涤:孵育完毕,用洗板机将所有孔中的液体吸出,然后在每孔内加满洗涤液。如此重复3次。最后,用洗板机吸出所有孔中洗涤液,在多层纸巾上将酶标板反放拍干,以去除残液。
(3)加入偶联抗体 根据使用说明,用偶联抗体结合稀释剂溶解抗体粉末得到抗体贮存液,于2~8℃贮存。
取240μL偶联抗体贮存液,加入到21mL偶联抗体稀释剂中得到偶联抗体工作液,于2~8℃贮存。
在每孔中加100μL偶联抗体工作液,封闭酶标板,轻轻摇晃混匀,37℃孵育1h。
(4)洗涤 洗涤方法同(2)。
(5)显色 每孔中加入100μL显色底物,轻轻摇动酶标板,室温孵育10min(加显色底物时应连续一次完成,不得中断,并保持相同次序和时间间隔)。
(6)终止反应 按照加入显色底物同样的顺序向酶标孔中加入100μL终止液,轻轻摇动酶标板10s,以终止颜色变化,并使终止液在孔中均匀分布(在加入终止液时应连续一次完成,不得中断,酶标板应注意避光,防止颜色深浅因受到光的影响而发生变化)。
(7)吸光值的测定 在加入终止液30min之内用酶标仪在450nm波长测量每孔的吸光值(OD)。
记录所得结果,用计算机软件处理。
(六)测试样品中目标蛋白浓度的计算
测试样品及参照标准的数值需减去空白样的数值,所测量的阳性标准品的平均值用于生成标准曲线,测试样品的平均值根据标准曲线计算相应浓度。
(七)结果可信度判断的原则
对于阳性标准品(大豆种子)而言,该方法检测的灵敏度必须保证在0.1%以上,定量检测的线性范围是0.5%~3%。
每一轮检测都必须符合表5-4所列的结果可信度判断的原则。每一轮反应应当包括空白、阴性标准品、阳性标准品和测试样品。所有样品检测液、空白对照都必须设置一个重复。如果不符合表5-4中所列的条件,所有检测实验需重新操作。
表5-4 结果可信度判断的条件
(八)ELISA方法检测转基因产品的优点和局限性
1.优点
特异性高,获得结果快,仪器简单,易于操作,对人员要求不高。免去了对样品进行核酸提取的麻烦,同时可降低检测的成本,由于酶具有很高的催化效率,可极大地放大反应效果,从而使测定达到很高的灵敏度和稳定性。
2.局限性
主要表现为:
①检测范围窄:ELISA分析需要转基因食品中含有待检测范围,如转EPSPS基因的耐除草剂大豆,转Bt基因的抗虫玉米等,因此只能在商业化GMF品种较少的情况下使用。目前商品化ELISA试剂盒只能检测少数几种GMF,且一种试剂盒只针对某一特定转基因产物,无法高通量、快速地检测具有多种混合成分的食品样品。
②易出现假阴性结果:一方面转基因食品中“新蛋白”含量通常很低,多数在10-12~10-6数量级水平,难以检出,另一方面蛋白质在食品加工过程中易变性,已加工食品中的蛋白质很可能失去抗体所针对的抗原表位,从而造成ELISA检测结果假阴性。此外蛋白质在受体生物基因组内表达前后如进行新的修饰,也可导致检测敏感性降低及假阴性结果。而有些转基因产品中的外源基因不表达蛋白质,则无法检测。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




