1.物理腐蚀
物理腐蚀是指当介质是液态金属时,由于液态金属对金属材料的单纯物理溶解作用而引起金属材料的破坏。例如,在热浸镀锌工艺中,熔融锌对铁制锅的腐蚀就属于物理腐蚀,腐蚀形成的新相是铁锌金属间化合物。
2.化学腐蚀
化学腐蚀是指金属表面与非电解质直接发生纯化学作用而引起的破坏。其反应过程的特点是,金属表面的原子与非电解质中的氧化剂直接发生氧化还原反应形成腐蚀产物,即氧化还原反应是在反应粒子相互作用的瞬间,于碰撞的那一个反应点上完成的。腐蚀过程中电子的传递是在金属与氧化剂之间直接进行的,因而没有电流产生。
纯化学腐蚀的情况并不多,主要为金属在无水的有机液体和气体中的腐蚀,以及在干燥气体中的腐蚀。
3.电化学腐蚀
电化学腐蚀是指金属表面与离子导电的介质(电解质)发生电化学反应而引起的破坏。任何以电化学机理进行的腐蚀反应至少包含一个阳极反应和一个阴极反应,并以流过金属内部的电子流和介质中的离子流形成回路。阳极反应是氧化过程,即金属离子从金属转移到介质中并放出电子;阴极反应为还原过程,即介质中的氧化剂组分吸收来自阳极的电子。
电化学腐蚀的特点在于,它的腐蚀历程可分为两个相对独立并可同时进行的过程。由于在被腐蚀的金属表面上存在着在空间或时间上分开的阳极区和阴极区,腐蚀反应过程中电子的传递可通过金属从阳极区流向阴极区,其结果必有电流产生。
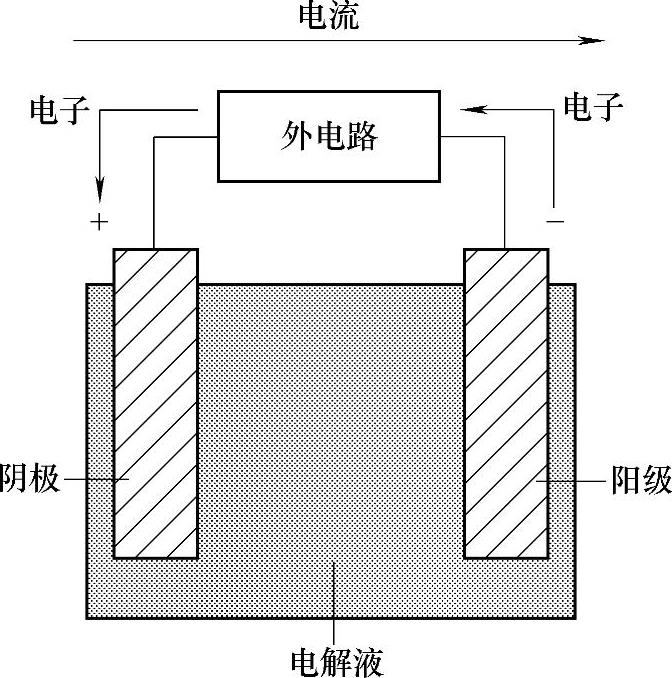
图1-1 双金属电偶原电池的结构
金属的电化学腐蚀实质上是短路的电偶电池作用的结果。这种原电池称为腐蚀电池。金属腐蚀的原电池有两种基本形式:双金属电偶和浓差原电池。图1-1所示为双金属电偶原电池的结构。该电池是由两种不同金属浸入一种电解质溶液组成的。当两电极由一种外部的、连续的、金属性质的通道连接起来时,便产生了电流。浓差电池是由两种相同的金属或合金所组成的阴极、阳极以及电流回路构成的。与金属接触的溶液的浓度不同,提供了产生电流的动力。在一个原电池中,导致腐蚀必须具备以下四个基本因素:
(1)阳极 这是阳极反应发生、产生电子的电极。腐蚀在阳极发生。
(2)阴极 阴极是接受电子的电极。阴极受保护而不会被腐蚀。
(3)电解质 电解质就是导体,离子流通过导体进行传输。电解质包括酸性、碱性和中性(盐)水溶液。(https://www.xing528.com)
(4)回路 回路是连接阳极和阴极的金属通路。它一般是基体金属。
阳极、阴极、电解质和回路都是腐蚀发生的必要条件。其中任何一个条件失去都会使电子流动停止,腐蚀将停止进行。如果阳极或阴极被另一种不同的金属所替代,就有可能导致电流流向的改变,从而改变受腐蚀的电极。
电化学腐蚀的基本过程包含下列三个过程:
(1)阳极过程 阳极过程是金属被溶解,以离子形式进入溶液中,电子留在金属上的过程,即
[Mn+·ne]→Mn++ne
(2)阴极过程 阴极过程是溶液中的氧化性物质(也叫去极化剂,D)在阴极表面接受从阳极流过来的电子的过程,即
D+ne→[D·ne]
许多种氧化性物质都可以在阴极表面上接受电子,但是最常见的接受电子的物质是氢离子和氧分子,由这两种物质接受电子引起的腐蚀分别称为析氢腐蚀和吸氧腐蚀。
(3)电流的流动 在腐蚀电池中,阳极区发生着阳极过程,阴极区发生着阴极过程。这两个过程靠电子的流动过程而紧密地联系着(电子经阳极流向阴极)。
在溶液中,阳离子向阴极区移动,阴离子向阳极区迁移。只要其中一个过程受到阻滞,其他两个过程也将不能顺利进行,整个腐蚀电池的工作受阻,金属的电化学腐蚀过程也难以顺利进行。
图1-2所示为腐蚀电池的工作原理。按照上述电化学过程,金属的腐蚀破坏将集中出现在阳极区,在阴极区将不发生可觉察的金属损失,它只起了传递电子的作用。
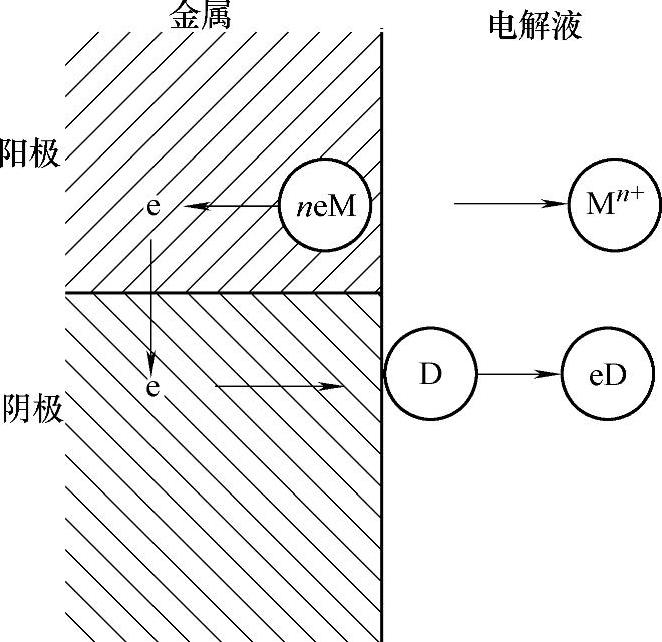
图1-2 腐蚀电池的工作原理
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




