1. 污水的水质指标
为了反映水体被污染的程度,要用污水的水质指标来表示。污水水质指标主要有下列几项:
(1)悬浮物,或称悬游物,是污水中呈固体状的不溶解物质。它是水体污染基本指标之一。
(2)废水中有机物浓度也是一个重要的水质指标。由于有机物的组成比较复杂,要想分别测定各种有机物的含量比较困难,一般采用下面几个指标来表示有机物的浓度:
①生物化学需氧量,简称生化需氧量,用BOD表示(Biochemical oxygen demand), BOD表示水中的有机污染物经微生物分解所需的氧量(单位体积的污水所消耗的氧量,毫克/升)。生化需氧量越高,表示水中需氧有机物质越多。
②化学需氧量(COD,即Chemical oxygen demand的缩写)用化学氧化剂氧化水中有机污染物时所需的氧量。COD越高,表示有机物质越多。目前常用的氧化剂主要是重铬酸钾或高锰酸钾。以高锰酸钾作氧化剂时,测得的值也称耗氧量。
③总有机碳(TOC,即Total organic carbor的缩写)和总需氧量(TOD,即Total oxygen demand的缩写)。
由于目前应用BOD测试时间长,不能快速反映水体被需氧有机物质污染的程度,国外在进行TOC,TOD的试验,以便寻求它们与BOD的关系,以实现自动快速测定。
(3)pH值
污水的pH值对污水处理及综合利用,对水中生物的生长繁殖,对排水管道等都有很大影响,所以被列为检验污水水质的重要指标之一。
生活污水pH值为7.2—7.6
工业污水的pH值就较复杂,变化较大。
(4)污水的细菌污染指标
1毫升污水中的细菌数要以千万计。其中大部分是寄生在已丧失生活机能的机体上,这些细菌是无害的;另一部分细菌,如霍乱菌、伤寒菌、痢疾菌等则寄生在有生活机能的活的有机体上,它们对人、畜是有害的。对污水进行细菌分析是一项很复杂的工作,在水处理工程中,用两种指标表示水体被细菌污染的程度:
① 毫升水中细菌(杂菌)的总数。
② 水中大肠菌的多少。水中含有大肠菌,即说明已被污染。
(5)污水中有毒物质指标
我国已制定过“地面水中有毒物质的最高容许浓度”的标准,列出了40种有毒物质。
以上五个指标是表示水体污染情况的重要指标,此外还有温度、颜色、放射性物质浓度等。也是反映水体污染情况的指标。
2. 水体污染源
水体污染来源有二种形式:
(1)点源——主要指工业污染源和生活污染源。其变化规律服从工业生产废水和城镇生活污水的排放规律。即季节性和随机性。
工业废水是水体最重要的污染源。它量大、面广、含污染物多,成分复杂,在水中不易净化,处理也比较困难。它具有下列特性:
①悬浮物质含量高,最高可达30000mg/l(而生活污水一般在200~500mg/l)。
② 需氧量高,有机物一般难于降解。对微生物起毒害作用。
COD为400~10000mg/l。
BOD为200~5000mg/l。
(生活污水BOD210~600mg/l)
③pH值变化幅度大,pH=2~13
④ 温度较高,排入水体可引起热污染。
⑤易燃:常含有低燃点的挥发性液体如汽油、苯、CS2、甲醇、酒精、石蜡等。
⑥ 多种多样的有害成分:硫化物、氰化物、汞、镉、铬、砷等。
另一个大的点源是城市生活污水。生活污水中物质组成与工业废水组成截然不同。它主要是日常生活中各种洗涤水,99.9%以上为水。固体物质小于1%,而且多为无毒物质。
生活污水的特点:
① 含氮、磷、硫高
在生活污水中有机物质主要有纤维素,淀粉、糖类、脂肪、蛋白质和尿素等。在厌气细菌作用下,易产生恶臭物质,如H2S、硫醇和3—甲基氮杂茚粪臭素)
② 含有大量合成洗涤剂,对人体可能有一定的危害。
③ 含有多种微生物,每毫升污水中可含几百万个细菌,病原菌也多。
(2)面源
农村污水和灌溉水是水体污染的主要面源。由于农田施用化肥和农药,灌溉后排出的水或雨后径流中,常含有农药和化肥,对水体影响很大,如农药污染、富营养化。在污水灌溉区,河流、水库、地下水均会出现污染。
面源的变化规律主要服从作物的分布和管理(农药、施肥)。
此外,由于地质溶解作用以及降水对大气淋洗,使污染物进入水体,这也是一种面源。
3. 水体中的主要污染物
对水体污染有较大影响的共有十种污染物:
(1)需氧污染物
生活污水和某些工业废水中所含的碳水化合物、蛋白质、脂肪和木质素等有机化合物可在微生物作用下最终分解为简单的无机物质,这些有机物在分解过程中需要消耗大量的氧气,故被称之为需氧污染物。需氧有机物是水体中最经常和普遍存在的一种污染物。
下面着重叙述一下需氧污染物对水质的影响:
① 溶解氧
溶解氧(DO)是水质的重要参数之一,也是鱼类等水生动物生存的必要条件。据美国1971年的统计:全年因水体污染使鱼类死亡达7000多万尾,其中2000余万尾是因水缺氧而致死的。一般鱼类生活所需的氧量视鱼种、发育阶段、活动强度和水温等因素而定。例如暖水鱼群每天至少应有16小时生活在DO>5ppm和8小时生活在DO>3ppm的水中。较优良的鱼种需氧量较多。由于各种因素的影响,水中DO含量变化很大,即在一天之中也不相同,主要影响因素有:再充气过程(Reaeration)、光合作用、呼吸和有机废物的氧化作用。再充气过程与水中的DO含量有关,当DO含量与水中氧的溶解差距越大时,氧从空气进入水中的量也越多。澎湃奔流的河水由于与空气交界面积较大,再充气的过程也比静止的水体为快。水中植物的光合作用在白昼进行并产生氧,也会使水中的DO增加。水生物的呼吸作用是全天不分昼夜地连续进行,并不断地从水中耗用氧而使DO减少。图10—1说明一天中水的DO含量随上述三种作用而变化的情况由图中曲线可知,早晨日出后由于光合和再充气同时作用,水中DO不断上升;但过了午后,因DO超过了溶解度,以致再充气过程发生逆转,氧倒从水中释出,从而曲线开始下降,傍晚日落后光合作用停止,因此曲线继续下降。
图10—1 水中DO随呼吸、光合和再充气作用而变化的情况
图10—2示出有机废物的氧化作用和DO含量的关系。当水体污染程度较低时,好气性细菌使有机废物发生氧化分解而逐渐消失,因此DO减少到一定含量后而不再下降。但如泥污比较严重,超过水体自净化的能力,则水中DO耗尽,从而发生厌气性细菌的分解作用,同时水面常会出现粘稠的絮状物使与空气隔开,妨碍再充气过程的进行。此时水中DO不足,可能引起鱼类等水生动物的死亡。
②生化需氧量BOD
图10—2 水体中有机废物与溶解氧含量的关系
图10—3 BOD余和BOD用随时间t而变化的情况
BOD应用时有两种形式,一是BOD用,表示经过时间t所耗用的氧量;一是BOD余表示该时刻水中所残余的生化需氧量。如图10—3所示,它们都随时间成指数函数而发生变化,或:
式中BOD总代表有机废物全部分解所需耗用的氧量,k表示分解氧化反应的速率常数。
有机废物中亚硫酸盐,亚硝酸盐和硫化物等在一天内可氧化完成;烃的氧化需7—10天才能完成。因此,目前水质标采用在20℃下分解5天(t=5)所需耗用的氧量,以BOD6表示,它通常是BOD总的70%左右,例如已知BOD5=200ppm,k=0.22/天。由式8—2求得:
BOD这一概念在水质管理中极为重要,例如一般生活污水的BOD5约为200ppm,工业废水的BOD5可高达数千ppm,在20℃时水中溶解氧的饱和浓度9.70ppm,显然,水中的DO很快就会耗尽而引起水生动物死亡和厌气分解。此外,含氮的有机废物约在10天左右分解释出氨,接着氨在硝化作用中氧化成亚硝酸盐和硝酸盐使BOD用突增。
③氧垂曲线(Oxygen Sag Curve)
图10—4 中的曲线中部成下垂形状,就是所谓氧垂曲线,它说明水体对需氧有机废物的天然自净化过程。当有机废物排入水体中时,由于细菌的氧化分解作用使水中DO下降,同时废物量也减少了。在另一方面,由于DO越来越低于氧在水中的溶解度,再充气过程也越来越快,使更多的氧由空气进入水中,当这两种相反的作用达到平衡时,DO下降和上升的速度相等,曲线就不再下垂;此后由于废物量越来越少,曲线反而开始上升,直到DO恢复正常为止。此时水体的自净过程即告完成,图中横坐标是下游的距离,废物是间断地分批加入的,如果废物连续地定量加入,则横坐标可用时间。
图10—4 氧垂曲线
(2)植物营养物
所谓植物营养物主要是指氮、磷、钾、硫及其化合物。从农作物生长的角度看,植物营养物是宝贵的物质,但过多的营养物质进入天然水体,将恶化水体质量,影响渔业的发展和危害人体健康。
水体中植物营养物的来源:
在地表水中,氮化合物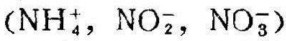 的总量一般不超过百分之几至十分之几mg/l,磷化合物
的总量一般不超过百分之几至十分之几mg/l,磷化合物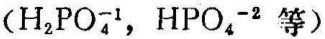 的数值也大致在这个范围内。天然水中过量的植物营养物质主要来自三个途径:
的数值也大致在这个范围内。天然水中过量的植物营养物质主要来自三个途径:
第一个途径,也是主要方面,来自化肥。据统计,在1963年全世界工业固氮量约3000万吨,到2000年将达1亿吨;1972年世界磷肥产量已达2109万吨。仅以1973年统计,荷兰每公顷(合15亩)N、P、K施肥量高达750公斤;比利时622公斤;新西兰612公斤;日本为440公斤。但施入农田的化肥只有一部分为农作物所吸收,以氮肥为例,在一般情况下,未被植物利用的氮肥超过50%,有的甚至超过80%。这样多的未被植物利用的氮化合物绝大部分被农田排水和地表迳流携带至地下水与地表水中。
第二个途径,来自生活污水的粪便(氮的主要来源)和含磷洗涤剂。由于近年来大量使用含磷洗涤剂,生活污水中含磷量显著增加。如美国生活污水中50—75%的磷来自洗涤剂。
第三个途径,由于雨、雪对大气的淋洗和对磷灰石、硝石、鸟粪层的冲刷,使一定量的植物营养物质汇入水体。
植物营养物污染的危害——水体富营养化。“富营养化”是湖泊分类与演化方面的概念,湖沼学家一致认为富营养化是水体衰老的一种表现。在湖泊演化过程中,富营养化起着重要作用,如图10—5表示富营养化作用引起湖泊生态系统的变化。
水体中植物营养物质含量的增加,将导致水生生物,主要是各种藻类大量繁殖。藻类过度旺盛的生长繁殖将造成水中的溶解氧急剧变化,使水体处于严重缺氧,而造成鱼类大量死亡。
图10—5 富营养化作用引起的湖泊生态系统的变化
一般讲,总磷超过20毫克/米3,或无机氮超过300毫克/米3即可认为水体处于富营养化状态(见表10—1)
表10—1 水体富营养化的分级、作用及其影响
注:×,××,×××,表示危害程度或大小。(https://www.xing528.com)
富营养化造成的危害是严重的,特别是湖泊、水库、内海、河口等水体,水流缓慢,停留时间长,既适于植物营养素的积聚,又适于水生植物的繁殖。富营养化对鱼类和人体健康的主要危害如下:
① 藻类繁殖引起死鱼。如据日本京都大学等18所大学联合调查,濑户内海有1/3海域完全没有生物生存。造成这种状况的重要原因之一是富营养化。獭户内海频繁发生“红潮”(藻类繁殖引起海水变红色),造成鱼类大量死亡,1972年8月17—21日,一次严重“红潮”死鱼达1420万尾,损失约71亿日元。
② 硝酸盐超过一定量时有毒性,亚硝酸盐又能在人体内与仲胺合成亚硝胺,有使人得癌症、生畸胎和影响遗传的危险。
一般说来,对于人为的富营养化现象,防治的方法多着重于限制氮和磷的供应来源,但是,一旦这种现象发生之后,就很难对氮加以控制。因为在富营养化的水体中,藻类群落以兰绿藻占优势,它们能吸收空气中的氮、而且死后还会分解而释出氮,供其它藻类种群食用。这样,防止富营养化的关键就在于控制磷,但现今水体中磷的含量约有一半来自人们生活中使用的合成洗涤剂。
(3)重金属
在环境污染方面所说的重金属主要指汞、镉、铅、铬以及类金属砷等生物毒性显著的重元素,也包括具有毒性的重金属锌、铜、钴、镍、锡等。
重金属以汞毒性最大,镉次之,铅、铬、砷也有相当毒害,有人称之为“五毒”。
采矿和冶炼是向环境中释放重金属的最主要污染源,此外不少工业部门也通过“三废”向环境中排放重金属。
重金属污染物最主要的特性是:在水体中不能被微生物降解,而只能发生各种形态之间的相互转化,以及分散和富集的过程。这些过程统称为金属迁移。重金属在水体中的迁移主要是下列物理化学作用:
① 沉淀作用。重金属生成氧化物,或磷化物、碳酸盐等而沉淀,并大量聚集在排水口附近的底泥中,成为长期的次生污染源。
② 吸附作用。天然水体中含有丰富的胶体(各种粘土矿物、各种可溶性和不溶性的腐殖质等),能强烈吸附重金属离子。重金属在河流中的迁移主要以吸附在悬浮物上被流水搬运;这是使许多微量重金属转向固态的最重要途径。
此外还有氧化还原作用(如三价铬被氧化为六价铬,六价铬毒性远大于三价铬)、络合作用等。
从毒性和对生物体、人体的危害方面看,重金属的污染有三个特点:
(ⅰ)在天然水体中只要有微量浓度即可产生毒性效应,一般重金属产生毒性的范围大致在1~10毫克/升,毒性较强的金属如汞、镉产生毒性的浓度范围在0.01~0.001毫克/升。
(ⅱ)通过食物链的生物放大作用,重金属可以在较高级生物体内成千、成万倍地富集,然后通过食物进入人体,在人体某些器官中积累造成慢性中毒(在第二章讲食物链时已举了例子)。
日本发现的“骨痛病”是镉积累过多,引起肾脏功能失调,骨中钙被镉取代,骨骼软化,此病潜伏期很长,可达10—30年。
(ⅲ)水体中的某些重金属可在微生物的作用下转化为毒性更强的金属化合物,如汞的甲基化(无机汞在水环境或鱼体内由微生物的作用转化为毒性更强的有机汞,又叫甲基汞)。
(4)农药
第四章中已作介绍,此不重复。
(5)石油
将在本章“海洋污染”一节中详细介绍。
(6)酚类化合物
水体中酚的来源主要是冶金、煤气、炼焦、石油化工、塑料等工业排放的含酚废水。由于各工业的原料、工艺、产品不同,各种含酚废水的浓度、成分、水量都有较大的差别。如城市煤气站含酚废水可分高浓度和低浓度二种:
高浓度——含挥发酚2300—3000毫克/升
含不挥发酚700—2000毫克/升
低浓度——含挥发酚40—60毫克/升
含不挥发酚10—20毫克/升
又如石油加工厂含酚废水的主要特征是含酚量低,通常为50毫克/升左右。
另外,粪便和含氮有机物的分解过程中也产生少量酚类化合物,所以城市生活污水也是酚污染物的来源。
水体中酚类化合物的危害:
在西德、荷兰边境的莱茵河中年平均含酚量高达容许浓度的50倍。酚有毒性,但人体有一定解毒能力。如经常摄入的酚量超过解毒能力时,人会慢性中毒,而发生呕吐、腹泄、头疼头晕、精神不安等症状。水中含0.1~0.5毫克/升酚时,对鱼类虽然无直接毒害,但能使鱼肉带异味而影响食用。水中含酚超过0.002~0.003毫克/升时,如用氯法消毒,消毒后的水有氯酚臭味,影响饮用。
根据酚在水中对人的感官影响,一般规定饮用水挥发酚浓度为0.001 毫克/升水源的水中最大容许浓度可以是0.002毫克/升地面水最高容许浓度为0.01 毫克/升酚类属于可被天然分解的有机物,其中挥发性酚易被分解为无毒化合物。
(7)氰化物
水体中氰化物主要来自化学、电镀、煤气、炼焦等工业排放的含氰废水。对我国各地氰化电镀车间废水的实际调查,含氰废水中氰的浓度一般在20~70毫克/升化肥厂煤气洗气含氰约108毫克/升。
氰化物是剧毒物质,一般人只要误服0.1克左右的氰化钾或氰化钠便立即死亡。含氰废水对鱼类有很大毒性,当水中CN﹣含量达0.3~0.5毫克/升时,鱼可死亡。世界卫生组织订出了鱼的中毒限量为游离氰0.03毫克/升;
生活饮水中氰化物不许超过0.05毫克/升;
地面水中最高容许浓度0.1毫克/升;
水体对氰化物有较强的自净作用,天然水体中氰化物的净化过程主要有二个途径:一个是挥发排出,即通过下述反应转变为可挥发的氰酸:
这一过程的净化量可以占到水体对氰化物总自净量的90%左右;另一过程是氧化分解(即生物化学氧化):
在一般天然水条件下,微生物氧化过程所造成氰的自净量只占水体对氰化物总自净量的10%左右。夏季(温度高,光照良好)微生物氧化过程的自净量可以达到30%左右。
(8)酸碱及一般无机盐类
酸性废水主要来自三个方面:
①矿山排水——酸性废水主要来源之一,美国水体中的酸70%来自矿山排水,主要是由硫化矿物的氧化作用产生:
② 冶金和金属加工酸洗废水。
例如,日本工业每天用H2SO4两万吨,其中一半以上用于酸洗。
③雨水淋洗含SO2烟气后流入水体,形成酸雨。
酸雨问题是瑞典气象学家在50年代发现的,现在不少地区常下这种酸雨。在美国的东部地区,有时酸雨甚至达到醋酸那样的酸度。酸雨可使SO2等对大气的污染转移到对水体和土壤的污染。
碱性废水主要来自碱法造纸、人造纤维、制碱、制革等工业废水。
酸、碱废水彼此中和,可产生各种盐类,它们分别与地表物质反应也能生成一般无机盐类;所以酸和碱的污染,也必然伴随着无机盐类污染。
酸、碱废水破坏水体的自然缓冲作用,消灭或抑制细菌及微生物的生长,妨碍水体的自净功能,腐蚀管道和船舶。酸碱污染不仅能改变水体的pH值,而且可大大增加水中的一般无机盐类和水的硬度。
(9)放射性物质
大多数水体在自然状态下都有极微量的放射性。第二次世界大战后,由于原子能工业,特别是核电站的发展,水体的放射性日益增高。
放射性物质主要来源有三个途径:
① 核电站,为了解决能源问题,发达国家愈来愈多的发展原子能电站,据国际原子能局资料,1979年世界总发电量10亿瓩中原子能发电站为2400万瓩,占2.4%;预计到1985年原子能发电站将增至8亿瓩;至2000年时,可能达到40亿瓩,将超过预计世界总发电量70亿瓩的一半。原子能电站的迅速增多,必然会带来放射性污染问题。
放射性废水经浓缩后,有的用混凝上固化,装入容器内(如钢筋混凝土的大盒子或金属缸)投入到海中。如果容器破损,放射性污染物质漏出就造成对水体的污染。
如美国加利福尼亚州旧金山湾海岸外56公里的海中,从1946~1965年之间投弃了约47500桶放射性废弃物,到1976年经过海底调查和摄影,证明一部分桶罐破坏,漏出高浓度放射性物质。
② 核武器的试验,主要是大气中放射性尘埃的降落和地面径流。
③ 放射性同位素在化学、冶金、医学,农业等部门的广泛应用,随污水排入水体。
放射性污染物质的危害:
1970年由大气进入海洋的放射性物质总量约为2—6亿居里。现在世界任何海区均可测出锶—90和铯—137;北半球高于南半球。
污染水体的最危险放射性物质有锶﹣90,铯—137等。这些物质半衰期长,化学性能与组成人体的主要元素钙、钾相似,经水和食物进入人体后,能在一定部位积累,增加对人体的放射性辐照,可引起遗传变异或癌症。
另外,有时放射性物质在水环境中虽然不多但能经水生食物链而富集。如英国温斯克尔(Windscale)放射性废物工厂处理地,其附近海域食用海产中含放射性比较高。鱼含铯﹣137为300—1000微居里/公斤鲜重,贝类含钌﹣106为10000—100000微居里/公斤鲜重,比整个英国沿海平均高300—1000倍。美国哥伦比亚河一个地区调查资料表明,自排入大型原子能反应堆废水后,海中浮游生物所含的放射性物质大大增加,约为河水的2000倍,其中30—50%是磷﹣32,有些小鱼含磷﹣32为河水含磷﹣32的15万倍。
放射性同位素最主要的特点是蜕变,衡量其蜕变的快慢用半衰期(一种放射性物质中所含某一放射性原子的数目经由衰变减少到一半所需的时间)表示。如铀﹣238的半衰期是4.5×109年;钍—234的半衰期24.1 日;钋﹣218的半衰期3.05分;钋﹣214的半衰期1.5×10﹣4秒。这是放射性物质的最重要性质,用外部的物理作用并不能改变它们的放射强度,只有时间才能做到这一点。因此,对放射性物质的废水处理方法,就是以上面的特性为基础的。
(10)病原微生物和致癌物
水体中病原微生物主要来自生活污水和医院废水、制革、屠宰、洗毛等工业废水、以及牧畜污水。病原微生物有三类:
① 病菌——可以引起疾病的细菌。如大肠杆菌、痢疾杆菌、绿脓杆菌等。
② 病毒——一般没有细胞结构,但有遗传、变异、共生、干扰等生命现象的微生物。多数用电子显微镜才能观察到。如麻疹、流行性感冒、传染性肝炎病毒等。
③寄生虫——动物寄生物的总称。如疟原虫、血吸虫、蝈虫等(其中许多不是微生物)。
病原微生物是水体污染中主要的污染物,对人来讲,传染病的发病率和死亡率均很高。如印度德里市1955—1956年发生一次传染性肝炎,全市102万人口,将近10万人患肝炎,其中黄胆型肝炎29300人。
又如美国纽约港口在本世纪六十年代后期,水中细菌量较50年代后期增加了十倍。
含病原微生物的污水中均含有需氧有机物,因为需氧有机物能提供病原微生物生存所需的营养。因此,在处理病原微生物的污染时,必须首先处理需氧有机物对水体的污染,然后再考虑其它措施(如消毒)。
致癌物:前面讲的污染物质中大部分都含有致癌物质,如炼焦废水中的焦油含有多种致癌芳香烃;印染废水中染料有多种芳香胺类致癌物,象联苯胺,2—萘胺(均可致膀胱癌);植物营养物中的亚硝基化合物(向各种胺类、亚硝酸盐转化)有强烈的致癌性,能致肝癌;农药中有机氯化合物,如DDT、六六六等对小鼠动物试验证明能致肝癌、艾氏剂能使大白鼠患细胞癌、胆管癌;重金属中铬、镍致癌,后者可致肺癌;水体中的某些藻类和嫌气细菌合成有毒物质,其中有致癌物质。海底中嫌气细菌可合成3,4——苯并芘致癌物质。
癌症是当前人们谈虎色变的问题,特别是环境污染带来的致癌物已引起广泛的重视。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。




